Блокнот Больного ВЗК. IBD NOTE.МенюАнализ крови АСЦА, АНЦА
Подвиды АНЦА васкулитов
К васкулитам АНЦА в медицине относят несколько разновидностей васкулитов. Каждый из них поражает определенные органы и крайне опасен для организма человека. Выделяют такие разновидности ААВ:
Гранулематоз Вегенера. В этом случае страдают респираторные пути: слизистые органов слуха, зрения и дыхания. В некоторых случаях поражаются даже легкие. Болезнь развивается крайне стремительно. Если не принять меры, летальный исход наступает уже в течение первых 6–12 месяцев от начала патологии. Гранулематоз Вегенера бывает генерализованным и локальным. В некоторых случаях медики считают эти виды стадиями болезни. В ходе гранулематоза Вегенера на слизистых пациента образуются своеобразные наросты по типу полипов. С течением болезни они распадаются, образуя кровоточащие раны. Именно поэтому у пациента иногда выявляют легочное или иное кровотечение.
Важно: В некоторых случаях у пациентов страдают почки. Поражение мочевыделительных органов приводит к развитию быстропрогрессирующего гломерулонефрита
Почки некротизируются максимально быстро.
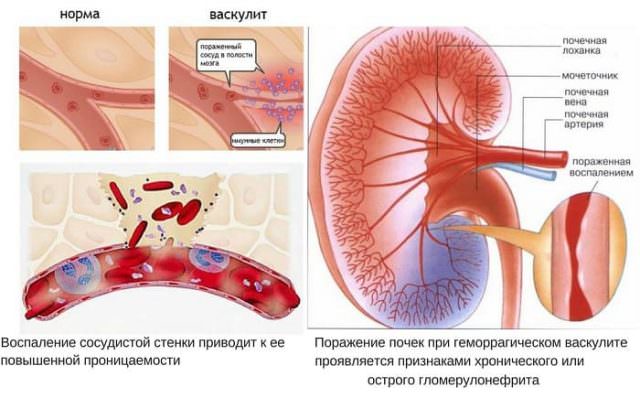
- Микроскопический полиангиит (МПА). Страдают мелкие и реже средние кровеносные сосуды внутренних органов. В основном поражаются почки, легкие, желудочно-кишечный тракт. В ходе прогрессирования болезни возникают внутренние кровотечения в легких, почках, органах ЖКТ. Иногда отмечаются неврологические симптомы заболевания в виде мононеврита. Сердце при МПА страдает реже.
- Эозинофильный гранулематозный полиартериит (ЭГПА). Болезнь еще называют синдромом Черджа–Стросс. В ходе такой разновидности АНЦА-васкулита страдают респираторные органы. Гранулемы на слизистой имеют выраженную эозинофильную инфильтрацию. То есть на слизистой образуются уплотнения и наросты из подвида лейкоцитов — эозинофилов.
Все виды ААВ являются серьезной проблемой для современной медицины, поскольку на начальных этапах заболевание практически никак не проявляется. Позднее, при явных признаках и симптомах, болезнь схожа со многими патологиями, что затрудняет проведение дифференциальной диагностики. Пока теряется драгоценное время на постановку диагноза, пациент как минимум превращается в инвалида. В худшем случае наступает летальный исход.
Симптомы болезни
В зависимости от классификации ААВ клиническая картина при разных его видах гетерогенна, то есть разнообразна. Выглядит симптоматика так:
- ГВ (гранулематоз Вегенера). Начало патологии характеризуется проявлением общей слабости и потерей аппетита. Позднее присоединяются повышенная температура тела, миалгия и слабость суставов (артралгия). Далее симптоматика зависит от пострадавшего органа-мишени. Если это глаза, то страдают радужка и белочная оболочка. Если это дыхательные пути, то сначала проявляется устойчивый насморк с гнойными выделениями. Не исключена перфорация носовой перегородки. Могут появиться кровохарканье, язвенный стоматит, гнойные выделения из ушей по типу отита. При поражении легких у пациента отмечаются одышка, плеврит и пр. Если же мишенью ГВ стали почки, то у пациента в моче явно видна кровь, отмечена высокая концентрация белка и при этом анализ на гемоглобин отрицательный. То есть его уровень критически снижен.
- Микроскопический полиангиит (МПА). В большинстве случаев у пациента проявляются поражения почек в виде стремительно прогрессирующего гломерулонефрита. Симптомы — кровь в моче, повышенный белок, болезненность в области поясницы. При поражении органов ЖКТ не исключен стул с примесью крови или рвотные массы с кровью.
- ЭГПА. В этом случае ко всем приведенным выше симптомам примешивается эозинофильный мио- или эндокардит, перикардит, гипертензия артериальная. На коже проявляются подкожные узелки, папулы. Со временем из папул образуются язвы. Отмечаются боли в животе при поражении органов ЖКТ.
Важно: причинами летальных исходов при ААВ становятся острая почечная или сердечная недостаточность, остановка кровообращения, сильное внутреннее кровотечение, дыхательная недостаточность
Механизм развития патологии
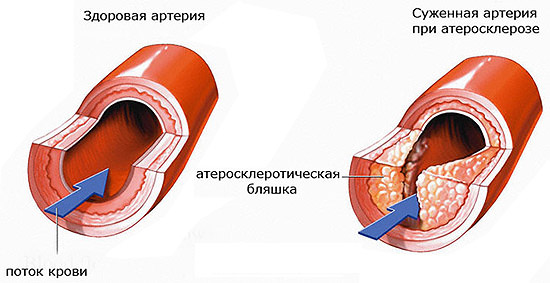
Все ААВ происходят на фоне аутоиммунных процессов в организме. По невыявленным причинам организм пациента начинает вырабатывать аутоантитела к клеткам кровеносных сосудов. В результате развивается воспаление стенок сосудистого русла. Просвет сосудов сильно сужается, что препятствует нормальному питанию органов-мишеней. От этого возникает ишемия тканей, питаемых данными сосудами. На фоне ишемии у пациента начинается некроз тканей и как следствие полный отказ органа.
Ученые выделяют несколько форм развития ААВ:
- Ограниченная. Характеризуется поражением исключительно верхних дыхательных путей.
- Генерализованная ранняя. Поражаются лишь сосуды без признаков нарушения работы внутренних органов.
- Генерализованная активная. Явно проявляются сбои в работе внутренних органов.
- Тяжелая. Налицо тяжелая декомпенсированная недостаточность внутренних органов на фоне васкулита АНЦА.
- Рефрактерная. Считается окончательной, поскольку добиться ремиссии при ней уже не удается даже на фоне грамотного и своевременного лечения.
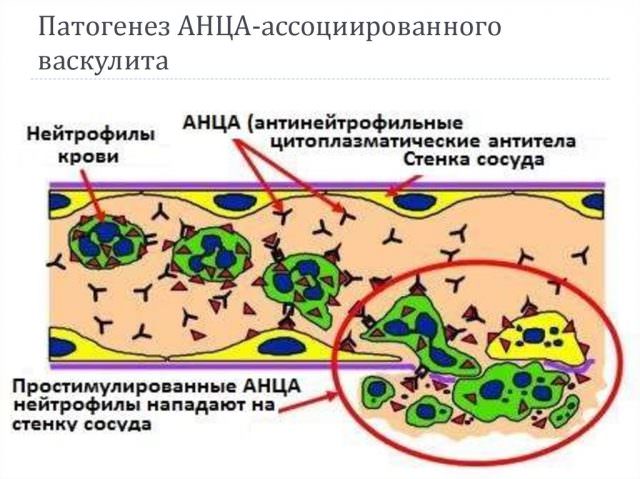
Этиология и патогенез
Этиология АНЦА-СВ неизвестна. К основным триггеров развития АНЦА-СВ относятся: генетическая предрасположенность, инфекционные возбудители (вирусы, бактерии, грибы, паразиты), экологические факторы, аллергены, медикаменты.
Патогенез АНЦА-СВ является мультифакториальные и до конца не выяснен. АНЦА-СВ является аутоиммунными заболеваниями, в основе которых лежат нарушения клеточного и гуморального иммунитета. АНЦА со специфичностью к ПР-3 или МПО характерны для АНЦА-СВ и играют ведущую роль в развитии этих заболеваний. Для ЕГПА и МПА характерна продукция АНЦА со специфичностью к МПО, тогда как для ГПА — со специфичностью к ПР-3. АНЦА обусловливают активацию нейтрофилов, которые играют роль в повреждении эндотелия, тканей и развития воспаления с высвобождением провоспалительных медиаторов, протеолитических ферментов и активных форм кислорода и инициацией агрегации тромбоцитов и тромбообразование. Особенностью патогенеза ЕГПА является аутоиммунный процесс с привлечением эозинофилов.
Лечение патологии
Главной целью лечения системного васкулита АНЦА является достижение стойкой ремиссии. Поэтому терапию делят на три этапа:
- Индукция ремиссии. Здесь используют в основном глюкокортикоиды типа преднизолон и метилпреднизолон. Препараты вводят внутривенно методом капельниц и внутрь в виде таблеток. Как правило, улучшение наступает в течение первых трех недель лечения. Но расслабляться не стоит. Поддерживающая терапия показана каждые четыре недели.
- Поддержание ремиссии. На этом этапе продолжают введение циклофосфамида для поддержания стойкого результата. Также используют препараты метотрексат или азатиоприн. На сегодняшний день ученые изучают эффективность лефлуномида и микофенолата мофетила.
- Терапия эскалационная. Направлена на восстановление функций пострадавшего органа. Лечение подбирают в зависимости от сложности состояния пациента и внутреннего органа-мишени.
Микроскопический полиангиит
При МПА в патологический процесс вовлекаются сосуды мелкого калибра (капилляры, венулы, артериолы), однако могут поражаться и сосуды среднего калибра.
Распространенность МПА меньше, чем ГПА, и болеют чаще мужчины старше 50 лет. Типичным является вовлечение в патологический процесс почек и легких, однако при МПА могут поражаться нервная система, кожа, опорно-двигательный аппарат, глаза, желудочно-кишечный тракт, а также сердце. Поражение ССС менее изучено при МПА, является не характерным и диагностируется в 10-20% случаев. Впрочем, данные о большей частоте развития патологии сердца у таких больных. Так, по данным исследования с участием 85 пациентов с МПА, в 50,6% было выявлено патологии сердца. Признаки СН выявлено в 17,6% больных, перикардит — в 10,6%, АГ — у 34%, ИМ — в 2,4%. Смертность пациентов, находившихся на лечении ГК и циклофосфамидом, составила 24,1%, при лечении только ГК — 48,4% (р
При МПА возможно развитие тампонады сердца, недостаточности аортального клапана, острой СН, изредка наблюдают поражения сердца вследствие неконтролируемой вторичной артериальной гипертензии. H. Tahir и соавт. описали у пациента с МПА с поражением легких и острым повреждением почек развитие суправентрикулярной тахикардии, неустойчивой желудочковой тахикардии с положительным эффектом применения ГК, циклофосфамида и плазмафереза. Описан случай стресс-кардиомиопатии такоцубо в 70-летнего пациента с активным МПА и полным регрессом симптомов поражения сердца после лечения ГК.
С помощью МРТ-ангиографии и МРТ с контрастом у пациентов с МПА, в которых отсутствовали симптомы поражения сердца, в 25% случаев выявлено фузиформни аневризмы, у 87,5% — эктазии коронарных артерий и в 12,5% — некроз миокарда.
Следует заметить, что патология сердца существенно ухудшает прогноз, особенно у пациентов с МПА. Основными причинами смерти были острая СН, нарушения ритма сердца, ИМ.
Какова роль этих анитиел в патогенезе васкулитов
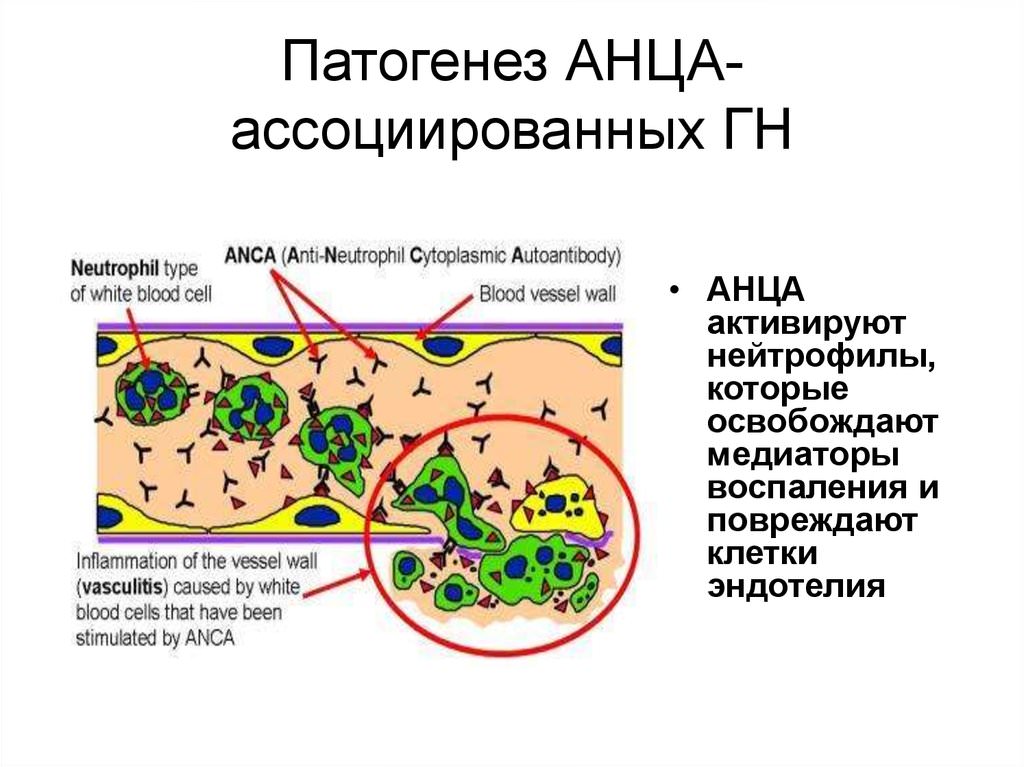
Современными данными установлено, что антитела к цитоплазме нейтрофилов играют важную роль в повреждении внутренней стенки сосудов, или эндотелия. В результате возникает биохимический каскад, затем выработка противовоспалительных цитокинов и развитие иммунного воспаления.
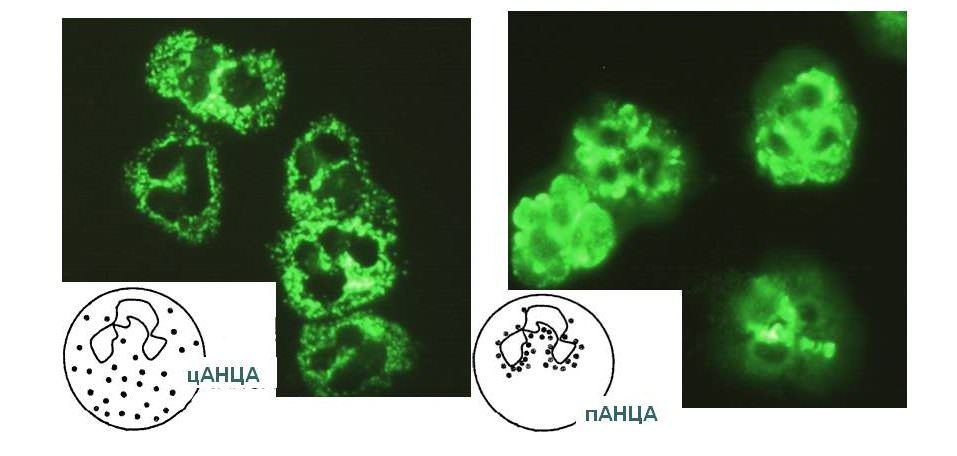
Выше было сказано, о том, что имеется два типа антител — цитоплазматические и перинуклеарные. Именно первый тип антител более сильно связан с одной из самых широко распространенных иммунных васкулитов, или гранулематозом Вегенера. Это анализ позволяет верифицировать заболевание у 85% пациентов. Но этот анализ все же является скрининговым, и отрицательный результат определения иммуноглобулинов вовсе не говорит о том, что у пациента нет системного васкулита.
С другой стороны, если у пациента уже установлен диагноз по другим стандартным критериям, то увеличение количества антител говорит или о рецидиве, или об обострении заболевания, а при успешной терапии это количество антител снижается. Можно сделать вывод, что этот анализ используется не только для диагностики, но и для контроля лечения.
Второй тип, а именно перинуклеарные антицитоплазматические антитела обнаруживаются у пациентов с быстропрогрессирующим поражением почек — гломерулонефритом. Позитивны они при системной красной волчанке, и хроническом язвенном колите.
Значения и интерпретация
Антитела к цитоплазме нейтрофилов у здорового человека не определяются, и, согласно единицам титрования, референсные значения должны быть меньше, чем 1 к 40. В том случае, если у пациента анализ показывает гораздо меньше разведение, например, 1к 100, то результат считается положительным.
Положительные значения, кроме названных болезней, может говорить о таком заболевании, как классический узелковый полиартериит, синдром Гудпасчера и язвенный колит. Высокий уровень антител встречается также при системной красной волчанки и синдроме Чарга-Стросса. Повышение значений может быть при болезни Шенлейн-Геноха, неспецифическом язвенном колите, различных аутоиммунных формах гепатита.
Нужно помнить, что у 6% здоровых людей могут быть положительные значения этих антител, и после этого необходимо проверять дополнительно пациента на причастность к иммунным васкулитам.
Лечение и прогноз
АНЦА-СВ потенциально смертельными заболеваниями даже в условиях проведения современной терапии. Со времен первых описаний ГПА считали фатальным заболеванием со смертностью 90% в течение первого года после установления диагноза. Однако проведение современной иммуносупрессивной терапии (применение ГК и циклофосфамида) в сочетании с адъювантной терапией (антигипертензивные препараты, почечно-заместительной терапии) привело к улучшению выживаемости пациентов. Так, 5-летняя выживаемость пациентов с АНЦА-СВ составляет примерно 80%. Однако следует отметить, что пациенты с АНЦА-СВ имеют высшее смертность по сравнению с популяцией. Результаты исследования с использованием базы данных первичной практики Великобритании показали, что риск смерти в 9 раз выше в первый год после диагностирования ГПА по сравнению с группой контроля. По результатам исследования C. Mukhtyar и соавт., 5-летняя выживаемость пациентов с ГПА, МПА и ЕГПА равна 74-91, 45-76 и 60-97% соответственно. Тяжелые поражения сердца, почек, легких и развитие инфекций являются основными причинами смерти пациентов с АНЦА-СВ. Частота рецидивов составляет около 50% в течение 5 лет и выше в ГПА, чем в МПа. Данные исследования показали, что преклонный возраст является предиктором резистентности к лечению, а наличие АНЦА со специфичностью к ТР-3 и поражения легких являются прогностическими факторами рецидива у пациентов с АНЦА-СВ. По данным исследования M. Catanoso и соавт., Выживаемость среди пациентов с ГПА значительно ниже по сравнению с контрольной группой (р 21 год (95% ДИ 15,60-27,86).
Поражение сердца считают независимым ФР смертности пациентов с АНЦА-СВ, и примерно в 50% случаев ЕГПА и ГПА смертность ассоциированная с поражением сердца. Данные исследования, проведенного MR Hazebroek и соавт., Показали худшую долгосрочную выживаемость пациентов с ЕГПА сравнению с контролем, тогда как прогноз при ГПА является благоприятным. Кроме того, наличие поражения сердца в больных с АНЦА-СВ является значимым предиктором как общей, так и сердечно-сосудистой смертности. Эти данные подтверждают результаты исследования A. Brucato и соавт., Согласно которым привлечение сердца в патологический процесс имеет неблагоприятный прогноз и является главной причиной смерти у 50% пациентов с ЕГПА.
Поражение сердца у больных ЕГПА может потребовать трансплантации сердца. Так, описано 9 случаев трансплантации сердца у пациентов с ЕГПА и кардиомиопатией. Несмотря на иммуносупрессивное лечение, гистологическое исследование показало наличие активного васкулита в 78% случаев. Показатель 5-летней выживаемости таких пациентов равнялся 57%, 44% пациентов умерли вследствие внезапной смерти в период от 3 до 60 мес (в среднем через 32 мес) после оперативного вмешательства.
Итак, поражения ССС при АНЦА-СВ часто имеет субклиническое течение и потенциально неблагоприятный прогноз. Поэтому междисциплинарный подход, ранняя диагностика и оптимальная терапия важны у пациентов с АНЦА-СВ и могут предотвратить развитие и прогрессирование патологии сердца.
Своевременная диагностика поражения ССС способствует раннему назначению иммуносупрессивного лечения, может значительно улучшить прогноз заболевания.
Общие прогнозы для пациентов с васкулитами АНЦА
В целом прогноз для пациентов с васкулитом АНЦА сложно назвать благоприятным. Но с усовершенствованием современной медицины показатели улучшаются. Жизненный прогноз для больных с ААВ зависит от формы развития болезни, своевременности поставленного диагноза и адекватности назначенного лечения
Кроме того во внимание стоит брать общее состояние организма пациента, его возраст и наличие дополнительных хронических заболеваний. Если говорить сухими цифрами, то прогноз для пациентов с ААВ выглядит так:
- Выживаемость при гранулематозе Вегенера в первый год от постановки диагноза составляет почти 85 %.
- В первые пять лет при ГВ выживаемость составляет около 65 %, при синдроме Черджа-Стросса около 65–70 %, при МПА — 46–54 %.
Важно: патология очень коварна и провоцирует летальность в первые 1–5 лет от момента выявления болезни. Основная рекомендация современных медиков звучит как «своевременность и срочность»
То есть пациент, подозревающий у себя развитие опасного недуга, должен как можно скорее обратиться к семейному врачу и пройти полную диагностику. Своевременно выявленную болезнь можно перевести в состояние стойкой ремиссии и тем самым продлить жизнь пациенту. Об этом гласит основное руководство к действию при подозрении на васкулит любой этиологии. При этом в медицине не исключены случаи чуда, когда сила веры в себя побеждает любую болезнь.
Основная рекомендация современных медиков звучит как «своевременность и срочность». То есть пациент, подозревающий у себя развитие опасного недуга, должен как можно скорее обратиться к семейному врачу и пройти полную диагностику. Своевременно выявленную болезнь можно перевести в состояние стойкой ремиссии и тем самым продлить жизнь пациенту. Об этом гласит основное руководство к действию при подозрении на васкулит любой этиологии. При этом в медицине не исключены случаи чуда, когда сила веры в себя побеждает любую болезнь.
Антинейтрофильные антитела ANCA к MPO, PR3, антитела к GBM IgG, качественное определение

Метод исследования: Иммуноферментный анализ.
Антинейтрофильные цитоплазматические антитела (АНЦА) – гетерогенная популяция аутоантител, специфичных к цитоплазматическим антигенам гранулоцитов. АНЦА – надежные серологические маркеры системных некротизирующих васкулитов сосудов мелкого калибра, также именуемых ANCA-ассоциированными васкулитами (AAV).
В оответствии с Номенклатурой васкулитов пересмотра 2012 года (Arthritis & Rheumatism, 2013) к ANCA-ассоциированным васкулитам относятся: гранулематозный полиангиит (гранулематоз Вегенера), эозинофильный гранулематозный полиангиит (синдром Черджа-Стросс), микроскопический полиангиит, васкулит гиперчувствительности, пурпура Шенлейна-Геноха, болезнь Бехчета, криоглобулинемический васкулит, васкулит при ревматических заболеваниях (СКВ, РA, ССД, болезнь Шегрена), кожный лейкоцитокластический васкулит.
Различают два основных типа антинейтрофильных антител – цитоплазматические, взаимодействующие с протеиназой 3 (PR3, ПР3), и перинуклеарные, направленные против миелопероксидазы (МРО, МПО).
Уровни анти-PR3 и анти-МРО коррелируют с клиническим статусом, они высоки в активную стадию заболеваний и снижаются во время ремиссии.
Антитела к базальной мембране клубочков (AТ к GBM) используются в диагностике синдрома Гудпасчера, который характеризуется гломерулонефритом, легочными кровотечениями и образованием антител к базальной мембране клубочков.
Диагностическое значение аутоАТ
| Системные васкулиты (ANCA-ассоцииррованные васкулиты): гранулематоз с полиангиитом (Вегенера), микроскопический полиангиит, узелковый полиартериит, эозинофильный гранулематоз с полиангиитом (Черджа-Строс) | |
| Антитела к MPO, PR3 | Антинейтрофильные цитоплазматические АТ (АНЦА, ANCA) – серологический маркер системных некротизирующих васкулитов сосудов среднего и мелкого калибра. Различают 2 основных типа ANCA – АТ, взаимодействующие с протеиназой 3 (ПР3, PR3), и АТ, специфичные в отношении миелопероксидазы (МПО, MPO). |
| Антитела к GBM | АТ к базальной мембране клубочка (GBM). Маркер быстропрогрессирующего гломерулонефрита. Одновременное обнаружение с ANCA указывает на плохой прогноз функции почек. |
Показания к исследованию:
- Диагностика ANCA-ассоциированных системных васкулитов и быстропрогрессирующего гломерулонефрита;
- Мониторинг состояния пациентов после проведения лечения;
- Дифференциальная диагностика системных аутоиммунных заболеваний.
Интерпретация результатов:
Референсные значения (вариант нормы):
| Антитела к MPO | не обнаружено |
| Антитела к PR3 | не обнаружено |
| Антитела к GBM | не обнаружено |
Интерпретация результата
- Обнаружено – свидетельствует о наличии специфических аутоантител;
- Не обнаружено – свидетельствует об отсутствии специфических аутоантител;
- Серая зона (пограничный результат) – рекомендуется повторить исследование не ранее, чем через 2 недели при отсутствии острых воспалительных заболеваний.
Результат лабораторного исследования не является диагнозом, интерпретация результатов проводится с учетом клинических проявлений и данных анамнеза.
- определение аутоантител проводится с целью подтверждения диагноза у пациентов с недостаточным количеством клинических критериев;
- обнаружение аутоантител при отсутствии клинических признаков не является достаточным для постановки диагноза аутоиммунного заболевания;
- отмечено нарастание частоты выявления аутоантител у лиц пожилого и старческого возраста, на фоне приема лекарственных препаратов, при вирусных и бактериальных инфекциях, злокачественных новообразованиях, у здоровых родственников больных аутоиммунными заболеваниями;
- при оценке клинического значения аутоантител необходимо учитывать стойкость и выраженность их гиперпродукции. Например, при инфекциях наблюдается умеренное транзиторное образование аутоантител, а при аутоиммунных заболеваниях – стойкая выраженная гиперпродукция.
Обращаем Ваше внимание на то, что интерпретация результатов исследований, установление диагноза, а также назначение лечения, в соответствии с Федеральным законом № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» от 21 ноября 2011 года, должны производиться врачом соответствующей специализации



 Белок в анализе мочи у женщин может появляться по разным причинам
Белок в анализе мочи у женщин может появляться по разным причинам
 У беременных, в силу их особого физиологического состояния, к этому списку добавляются другие причины, связанные с увеличением количества крови, жидкости в организме в целом и соответственно – нагрузки на почки:
У беременных, в силу их особого физиологического состояния, к этому списку добавляются другие причины, связанные с увеличением количества крови, жидкости в организме в целом и соответственно – нагрузки на почки: При здоровой мочеполовой системе урина представляет собой прозрачную жидкость желтого цвета. Примесей нет.
При здоровой мочеполовой системе урина представляет собой прозрачную жидкость желтого цвета. Примесей нет.
 У здорового человека в выделяемой жидкости отсутствуют какие-либо посторонние элементы, поэтому ее помутнение можно рассматривать как признак наличия:
У здорового человека в выделяемой жидкости отсутствуют какие-либо посторонние элементы, поэтому ее помутнение можно рассматривать как признак наличия:


 Сама женщина должна следить за своим рационом. Питание не только должно быть безопасным в плане содержания вредных веществ. Оно должно быть еще и сбалансированным, то есть с нормальным соотношением белков, жиров и разных групп углеводов. Ущемление организма в белковой пище, как и его перегрузка, может вызвать дисбаланс и нехватку необходимых аминокислот у развивающегося плода. Также следует употреблять достаточное количество жидкости (при нормальном функционировании почек – около 1,5–2 л в сутки; при нарушениях их работы и появлении отеков норму определяет врач).
Сама женщина должна следить за своим рационом. Питание не только должно быть безопасным в плане содержания вредных веществ. Оно должно быть еще и сбалансированным, то есть с нормальным соотношением белков, жиров и разных групп углеводов. Ущемление организма в белковой пище, как и его перегрузка, может вызвать дисбаланс и нехватку необходимых аминокислот у развивающегося плода. Также следует употреблять достаточное количество жидкости (при нормальном функционировании почек – около 1,5–2 л в сутки; при нарушениях их работы и появлении отеков норму определяет врач).
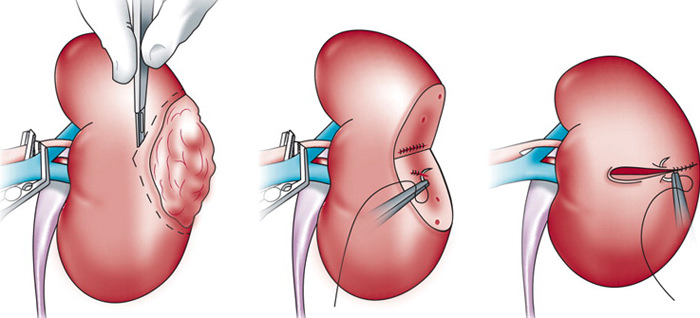
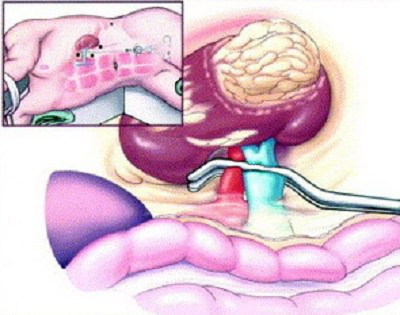 После остановки кровоснабжения осуществляют удаление левой или правой почки (по показаниям), расположенных вокруг тканей, лимфоузлов и надпочечника.
После остановки кровоснабжения осуществляют удаление левой или правой почки (по показаниям), расположенных вокруг тканей, лимфоузлов и надпочечника. Удаление почки при раке эффективно при условии отсутствия в кровеносных и лимфатических сосудах раковых клеток. Увеличить шансы позволяет химиотерапия, а также все чаще назначаемая сегодня иммунотерапия для активизации собственных защитных механизмов организма.
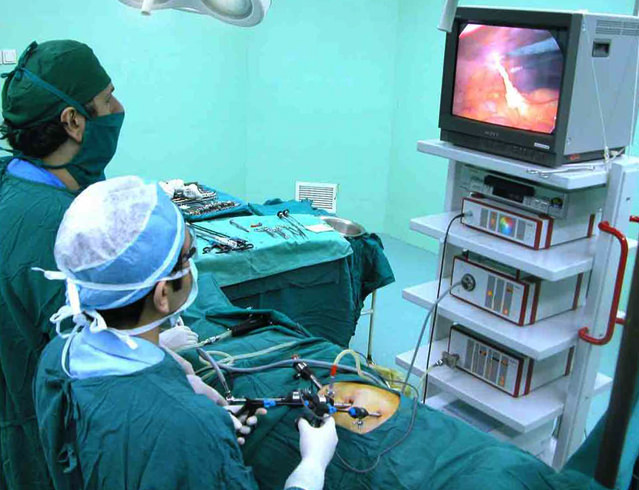
Удаление почки при раке эффективно при условии отсутствия в кровеносных и лимфатических сосудах раковых клеток. Увеличить шансы позволяет химиотерапия, а также все чаще назначаемая сегодня иммунотерапия для активизации собственных защитных механизмов организма.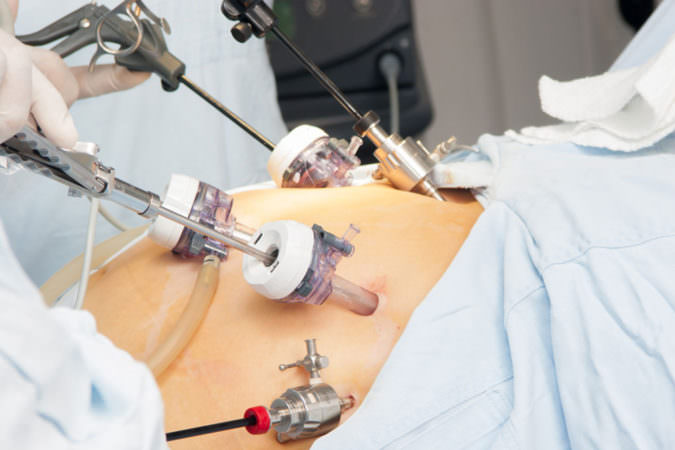 Лапароскопическая операция
Лапароскопическая операция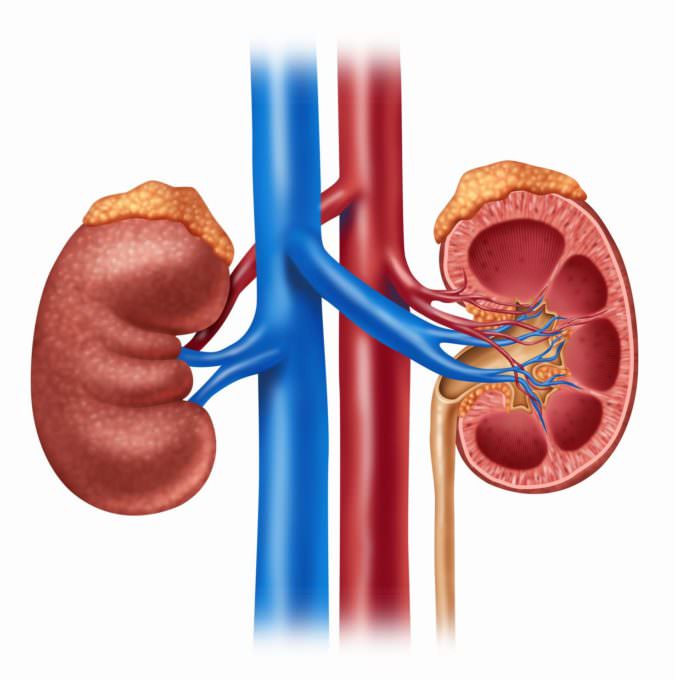 После удаления почки следует быть предельно внимательным к своему здоровью
После удаления почки следует быть предельно внимательным к своему здоровью Неотложные состояния Подробнее » Что такое уретральный свищ
Неотложные состояния Подробнее » Что такое уретральный свищ Одним из осложнений может быть кишечная непроходимость
Одним из осложнений может быть кишечная непроходимость
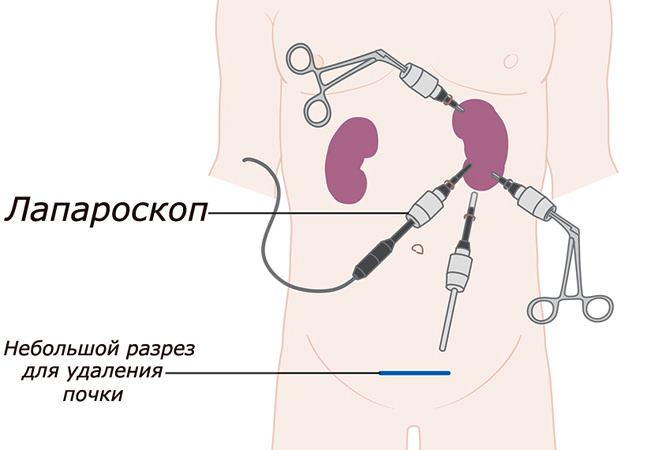
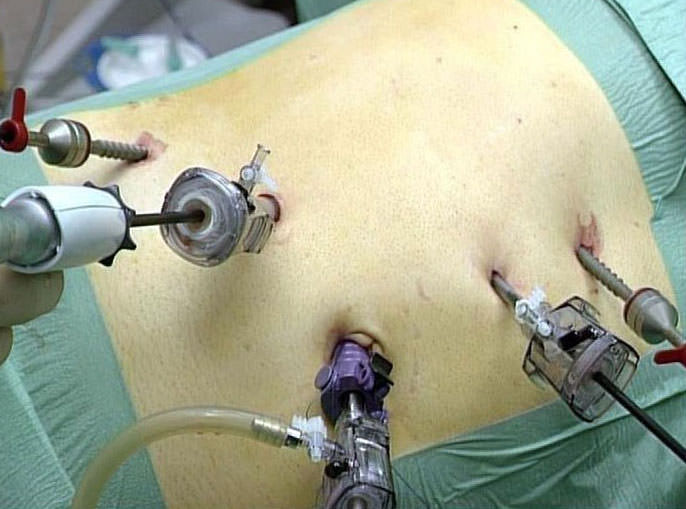 Лапароскопическая нефрэктомия
Лапароскопическая нефрэктомия Иногда проводят операции открытым способом
Иногда проводят операции открытым способом Удаление почки происходит с использованием специальных инструментов
Удаление почки происходит с использованием специальных инструментов








 Таким образом:
Таким образом:

 Процедура проведения плазмафереза
Процедура проведения плазмафереза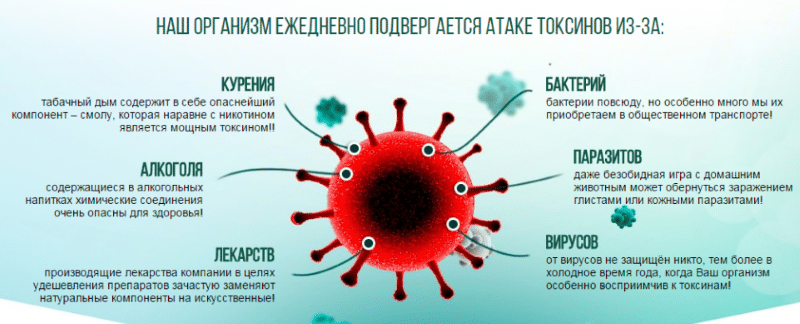 Причины попадания в кровь токсинов
Причины попадания в кровь токсинов
 Кровь и остальные компоненты внутренней среды организма, такие как лимфа и тканевая жидкость, находятся в тесном взаимодействии. Они ответственны за гомеостаз – постоянство состава и свойств биологических жидкостей. Находясь в динамическом равновесии, кровь и остальные компоненты внутренней среды организма являются взаимопревращаемыми.
Кровь и остальные компоненты внутренней среды организма, такие как лимфа и тканевая жидкость, находятся в тесном взаимодействии. Они ответственны за гомеостаз – постоянство состава и свойств биологических жидкостей. Находясь в динамическом равновесии, кровь и остальные компоненты внутренней среды организма являются взаимопревращаемыми. Часть крови, содержащейся в организме человека, циркулирует по сосудам, а часть – сосредоточена в депо, откуда она при необходимости может изыматься. Например, это происходит при кровопотерях. Кровяными депо являются:
Часть крови, содержащейся в организме человека, циркулирует по сосудам, а часть – сосредоточена в депо, откуда она при необходимости может изыматься. Например, это происходит при кровопотерях. Кровяными депо являются:





 Чтобы корректировать устную и письменную речь необходимо посещать логопеда. Психолог поможет восстановить психическое состояние больного. Если процесс реабилитации проходит не в медицинском учреждении, то необходимо постоянно наблюдаться у врача, ведь прогноз зависит от качества терапии.
Чтобы корректировать устную и письменную речь необходимо посещать логопеда. Психолог поможет восстановить психическое состояние больного. Если процесс реабилитации проходит не в медицинском учреждении, то необходимо постоянно наблюдаться у врача, ведь прогноз зависит от качества терапии. Если у человека парализовало правую сторону тела вследствие геморрагического мозгового кровоизлияния, то необходимо исключить любые физические нагрузки. Это объясняется тем, что чрезмерный кровоток может вызвать повторный приступ.
Если у человека парализовало правую сторону тела вследствие геморрагического мозгового кровоизлияния, то необходимо исключить любые физические нагрузки. Это объясняется тем, что чрезмерный кровоток может вызвать повторный приступ.
 Традиционные методы лечения не всегда доступны для кошелька каждого человека. Когда сил и нервов уже не осталось и использованы все существующие методы лечения левостороннего паралича, в борьбу вступает народный опыт и мудрость.
Традиционные методы лечения не всегда доступны для кошелька каждого человека. Когда сил и нервов уже не осталось и использованы все существующие методы лечения левостороннего паралича, в борьбу вступает народный опыт и мудрость.



 Нарушение мимики при инсульте
Нарушение мимики при инсульте 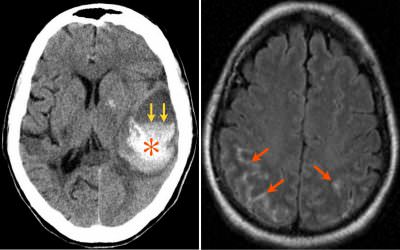 То, какая сторона будет подвержена обездвиживанию, зависит от локализации инсульта. Если паралич коснулся правой части тела, то патологическому влиянию подверглось левое полушарие. Обычно левосторонние инсульты сопровождаются не только гемипарезами, но и нарушениями речи.
То, какая сторона будет подвержена обездвиживанию, зависит от локализации инсульта. Если паралич коснулся правой части тела, то патологическому влиянию подверглось левое полушарие. Обычно левосторонние инсульты сопровождаются не только гемипарезами, но и нарушениями речи. Помощь при инсульте делится на два типа. Это базисное лечение и специфическое. Базисное лечение направлено на поддержание жизненно важных функций организма, таких как дыхание, нормальная работа сердца. Также нужно избежать отека мозга.
Помощь при инсульте делится на два типа. Это базисное лечение и специфическое. Базисное лечение направлено на поддержание жизненно важных функций организма, таких как дыхание, нормальная работа сердца. Также нужно избежать отека мозга. Лечение паралича при помощи лекарств, в случае локализации геморрагического инсульта в левом полушарии, подразумевает использование препаратов, способствующих лучшей свертываемости крови. Также накладывается ограничение на прием спазмолитиков и антиагрегантов.
Лечение паралича при помощи лекарств, в случае локализации геморрагического инсульта в левом полушарии, подразумевает использование препаратов, способствующих лучшей свертываемости крови. Также накладывается ограничение на прием спазмолитиков и антиагрегантов.