Венозная кровь
Почему вены синие, а не красные
На самом деле, конечно, вены хотя и несут темную бордовую кровь, в отличии от ярко-алой артериальной, они на цвет аж никак не синие. Они красные, как цвет крови, которая по них течет. И не стоит верить в теорию, которую можно встретить в интернете о том, что кровь на самом деле бежит по сосудам синяя, а при порезе и контакте с воздухом становится мгновенно красной – это не так. Кровь всегда красная, а почему описано выше в статье.
Вены лишь кажутся нам синими. Это объясняется законами физики об отражении света и нашим восприятием. Когда луч свет попадает на тело, то кожа отбивает часть всех волн и поэтому выглядит светлой, ну или другой, зависимо от меланина. Но синий спектр она пропускает хуже красного. А вот сама вена, а точнее кровь, поглощает свет всех длин волн (но меньше, в красной части спектра). То есть получается, что кожа дает нам для видимости синий цвет, а сама вена – красный. Но, интересно, что на самом деле вена отражает даже немного больше красного, чем кожа синего спектра света. Но почему тогда мы видим вены синими или голубыми? А причина, на самом деле, кроется в нашем восприятии – мозг сравнивает цвет кровеносного сосуда против яркого и теплого тона кожи, а в итоге показывает нам синий.
Почему же мы не видим другие сосуды, по которым течет кровь ?
Если кровеносный сосуд находится ближе 0,5 мм к поверхности кожи, то он вообще поглощает практически весь синий свет, а отбивает намного больше красного – кожа выглядит здоровой розовой (румяной). Если сосуд намного глубже 0,5 мм, то он просто не виден, ведь свет к нему не доходит. Поэтому и получается, что мы и видим вены, которые приблизительно расположены на расстоянии 0,5 мм от поверхности кожи, а почему они синие уже описано выше.
Почему мы не видим артерии из-под кожи?
На самом деле, около двух третей из объема крови находится в венах в постоянно, следовательно, они большего размера чем другие сосуды. Кроме этого у артерий значительно толще стенки, чем у вен, ведь им приходится выдерживать большее давление, что также мешает им быть достаточно прозрачными. Но даже, если бы артерии было видно из-под кожи также, как и некоторые вены, то предполагается, что они имели бы приблизительно такой же цвет, не смотря на то, что кровь бежит по ним более яркая.
Какого же на самом деле цвета вены?
Если вы когда-либо готовили мясо, то вероятно уже знаете ответ на этот вопрос. Пустые кровеносные сосуды красновато-коричневого цвета. Существует не так много различий в цвете между артериями и венами. Они отличаются в основном при рассмотрении в поперечном сечении. Артерии толстостенные и мускулистые, а вены имеют тонкие стенки.
Чем венозная кровь отличается от артериальной
Движение этой кровяной массы происходит совсем по-другому. Из правого желудочка сердца начинается малый круг кровообращения. Отсюда венозная кровь течет по артериям к легким.
Там она отдает углекислый газ и насыщается кислородом, превратившись в артериальный тип.По легочной вене кровяная масса возвращается в сердце.
Система вен более обширна, чем система артерий.Сосуды, по которым течет кровь, тоже отличаются.Так вена обладает более тонкими стенками, а кровяная масса в них немного теплее.
 Кровь в сердце
Кровь в сердце
- Артериальная масса ярко-красного цвета. Это объясняется тем, что она насыщена гемоглобином, который присоединил O2. Для В.К. характерен темно-бордовый цвет, иногда с голубоватым оттенком. Это говорит о том, что в ее составе высок процент углекислого газа.
- Согласно исследованиям биологии химический состав А.К. богат кислородом. Средний процент содержания O2у здорового человека – свыше 80 mmhg. В В.К. показатель резко падает до 38 – 41 mmhg. Показатель углекислого газа отличается. В А.К. он составляет 35 – 45 единиц, а в В.К. доля CO2колеблется от 50 до 55 mmhg.
 Артериальная и венозная кровь
Артериальная и венозная кровь
- Главная функция А.К. – обеспечить органы человека кислородом и полезными веществами. В.К. необходима для того, чтобы доставить углекислый газ в легкие для дальнейшего вывода из организма и для устранения прочих продуктов распада.
- Кровь по артериям большого кольца кровообращения и малого кольца движется с разной скоростью. А.К. выбрасывается из левого желудочка в аорту. Она разветвляется на артерии и более мелкие сосуды. Далее кровяная масса попадает в капилляры, питая всю периферию O2. В.К. двигается от периферии к сердечной мышце. Различия состоят в давлении. Так кровь выбрасывается из левого желудочка под давлением 120 миллиметров ртутного столба. Далее давление понижается, и в капиллярах составляет около 10 единиц.
- В медицине забор крови для развернутого анализа всегда берут из вены. Иногда из капилляров. Биологический материал, взятый из вены, помогает определить состояние организма человека.
Разница венозного кровотечения от артериального
Различить виды кровотечений несложно, это могут сделать даже люди, далекие от медицины. Если повреждена артерия, то кровь ярко-красного цвета.
Она бьет пульсирующей струей и вытекает очень быстро. Кровотечение сложно остановить.Это главная опасность повреждения артерий.
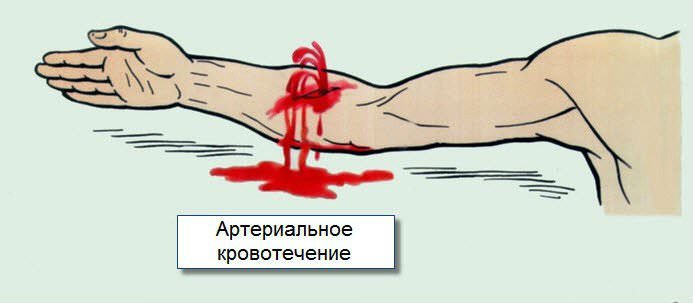 Артериальное кровотечение
Артериальное кровотечение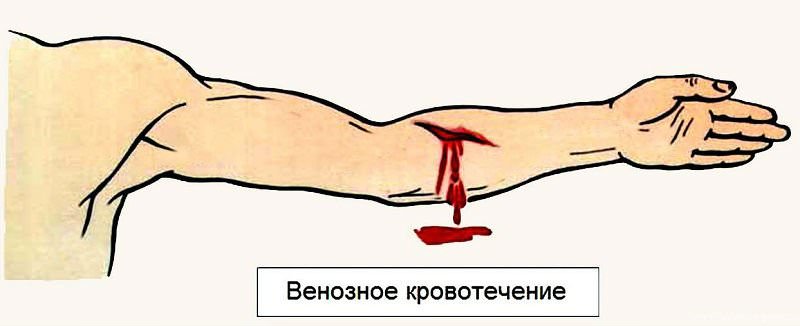 Венозное кровотечение
Венозное кровотечение
Оно не остановится без оказания первой помощи:
- Пострадавшую конечность следует поднять.
- Поврежденный сосуд, немного выше ранения зажать пальцем, наложить медицинский жгут. Но его нельзя носить более одного часа. Перед наложением жгута обернуть кожу марлей или любой тканью.
- Больного срочно доставить в больницу.
Артериальное кровотечение может носить внутренний характер. Это называется закрытая форма.В этом случае повреждается сосуд внутри тела, и кровяная масса попадает в брюшную полость или разливается между органами.Больному резко становится плохо, кожа бледнеет.
При кровотечении из вены жидкость вытекает медленной струей. Цвет – темно-бордовый. Кровотечение из вены может остановиться и самостоятельно. Но рекомендуется перебинтовать рану стерильным бинтом.
Забрав у них углекислый газ и элементы распада, кровь превращается в венозную. Она доставляет продукты метаболизма в легкие для дальнейшего устранения из организма.
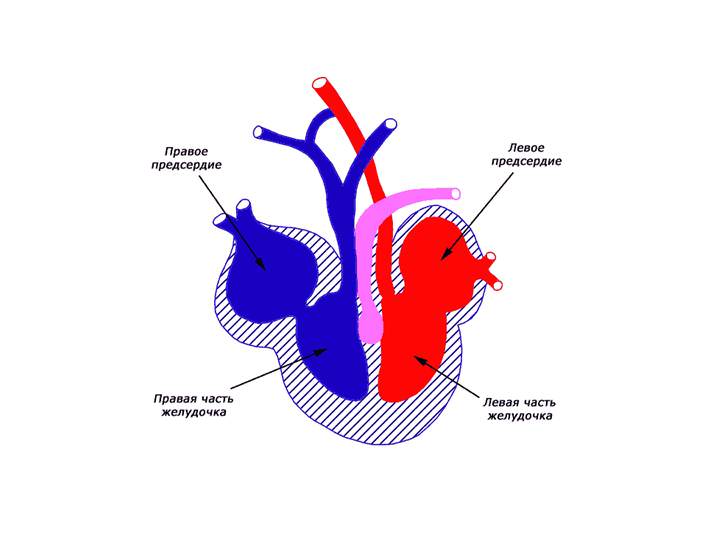
Механизмы разделения
Расположенные внутри сердца межпредсердная и межжелудочковая перегородки не позволяют артериальной крови смешиваться с венозной. При наличии дефекта перегородки или аномального строения сосудов случается ее смешивание или неправильное распределение в организме, что иногда выявляется у детей с врожденными пороками сердца. Патологии:
- Дефект межжелудочковой перегородки.
- Дефект межпредсердной перегородки.
- Открытый боталлов проток между аортой и легочной артерией.
- Тетрада Фалло — сочетание дефекта межжелудочковой перегородки с выходом аорты частично из правого желудочка и сужением легочной артерии.
Чтобы вовремя заметить какие-либо нарушения в организме, необходимы хотя бы элементарные знания анатомии человеческого тела
Глубоко внедряться в этот вопрос не стоит, а вот иметь представление о самых простых процессах очень важно. Сегодня давайте выясним чем отличается венозная кровь от артериальной, как она движется и по каким сосудам
Основной функцией крови является транспортировка питательных веществ к органам и тканям, в частности, поставка кислорода от лёгких и обратное перемещение углекислого газа к ним. Этот процесс можно назвать газообменом.
Циркуляция крови осуществляется в замкнутой системе сосудов (артерии, вены и капилляры) и делится на два круга кровообращения: малый и большой. Такая особенность позволяет разделить её на венозную и артериальную. В результате нагрузка на сердце значительно уменьшается.
Давайте разберём какая кровь называется венозной и чем она отличается от артериальной. Этот вид крови прежде всего имеет тёмно-красный цвет, иногда ещё говорят, что она отличается голубоватым оттенком. Объясняется такая особенность тем, что она переносит углекислый газ и другие продукты метаболизма.
Кислотность венозной крови, в отличие от артериальной, немного ниже, также она боле тёплая. По сосудам течёт медленно и достаточно близко к поверхности кожи. Это происходит из-за особенностей строения вен, в которых присутствуют клапаны, способствующие уменьшению скорости тока крови. Также в ней отмечается предельно низкий уровень содержания питательных веществ, в том числе и снижение сахара.
В подавляющем большинстве случаев именно этот тип крови используют для проведения анализов при каких-либо медицинских обследованиях.
При венозном кровотечении справиться с проблемой значительно проще, чем при аналогичном процессе из артерий.
Количество вен в человеческом теле в несколько раз превышает число артерий, эти сосуды обеспечиваю приток крови от периферии к главному органу – сердцу.
Артериальная венозная кровь
Артериальная и венозная кровь не смешиваются.
Азот содержится в артериальной и венозной крови в простом физическом поглощении по законам растворимости газов. Напряжение азота в крови соответствует парциальному давлению азота в альвеолярном воздухе.
|
Схема строения легких у XBOCTUTLIX амфлГшн ( / I, Л1 п рептилий ( / Л /. |
Однако перегородка эта неполная, и поэтому артериальная и венозная кровь в желудочке все-таки смешивается. Но телу, как н у амфибий, разносится не чистая артериальная кровь, а кровь, содержащая примесь углекислоты. Поэтому н у ящериц в связи с недостатком в кропи кислорода в теле образуется мало тепла, и жизнедеятельность животного зависит от внешних условии. Летом в жаркие дни ящерицы бодры п подвижны, в прохладную погоду они становятся более вялыми, а зиму проводят в спячке.
Полное ( как у птиц) разделений артериальной и венозной крови и сложная структура легких, образованных бесчисленным количеством легочных пузырьков, опутанных сетью капилляров ( вспомним мешковидные легкие лягушки), способствуют усиленному газообмену, с которым связана и теплокровность млекопитающих.
Открытие Лавуазье и Лапласа позволило объяснить различие в цвете артериальной и венозной крови.
|
Повышение концентрации ( показано штриховкой увеличенной частоты осмотически активных веществ в различных участках почки. |
А — теплообменник в сосудистой системе конечностей арктических животных; обмен тепла между артериальной и венозной кровью способствует сбережению тепла и на каждом уровне не превышает 1 — 2 С.
В красных кровяных тельцах до 20 % двуокиси углерода присутствует в форме карбамата и 45 / 0 разницы в содержании двуокиси углерода в этих клетках в артериальной и венозной крови вызвано сдвигом карбаминационного равновесия.
Именно так природа и поступает. Она уменьшает разность температур артериальной и венозной крови и за счет того, что артерии и веиы проходят, тесно соприкасаясь друг с другом.
При соединении гемоглобина с кислородом меняются не только свойства простетической группы, но и физические и химические свойства молекулы в целом. Ранее уже указывалось, что способность гемоглобина присоединять основания увеличивается при переходе гемоглобина в оксигемоглобин. Следствием этого является то, что артериальная и венозная кровь имеет почти одинаковую реакцию. Более высокое содержание угольной кислоты в венозной крови компенсируется более высокой кислотностью оксигемоглобина артериальной крови. Кривая образования оксигемоглобина в зависимости от давления кислорода характеризуется особой, необычной для подобных процессов, сигмо-образной формой ( фиг.
Льюис первым получил тяжелую воду ( оксид дейтерия ], которую теперь используют в качестве замедлителя в ядерных реакторах. Он обнаружил, что линии располагаются не совсем так, как было теоретически предсказано Полем Дираком. За эти исследования, явившиеся важным шагом на пути создания квантовой электродинамики, Лэмб в 1955 году был удостоен Нобелевской премии по физике вместе с Поликарпом Кушем. Кроме того, Людвиг создал устройство, измеряющее ток артериальной и венозной крови и исследовал функцию кислорода в крови. В 1893 году братья Огюст и Луи Жан ( 1864 — 1948) Люмьеры разработали конструкцию киноаппарата для съемки и проекции движущихся фотографий.
Последние образуют сложную сеть, из к-рой кровь поступает сначала в мелкие сосуды — венулы, а затем во все более крупные — вены. У круглоро-тых и рыб ( кроме двоякодышащих) имеется один круг кровообращения. По малому кругу венозная кровь из сердца по легочным артериям направляется в легкие и возвращается к сердцу по легочным венам. По большому кругу артериальная кровь направляется в голову, ко всем органам и тканям тела, возвращается по кардинальным или по полым венам. У всех позвоночных имеются воротные системы. С формированием малого круга кровообращения в процессе эволюции позвоночных осуществляется прогрессивная дифференцировка отделов сердца. У птиц и млекопитающих это привело к возникновению четырехкамерного сердца и к полному разделению в нем токов артериальной и венозной крови.
От чего зависит цвет крови
Красный цвет крови может иметь разные оттенки. Переносчики кислорода, то есть эритроциты (красные кровяные клетки), имеют оттенок красного в зависимости от гемоглобина – находящегося в них железосодержащего белка, который может связываться с кислородом и углекислым газом, чтобы переносить их в нужное место. Чем больше молекул кислорода соединено с гемоглобином, тем кровь более яркого красного цвета. Поэтому артериальная кровь, которая только обогатилась кислородом, такая ярко красная. После отдачи кислорода клеткам организма цвет крови меняется на темно-красный (бордовый) – такая кровь называется венозной.
Конечно, в крови содержатся и другие клетки, кроме эритроцитов. Это еще лейкоциты (белые кровяные тельца) и тромбоциты. Но они не в таком значительном количестве по сравнению с эритроцитами, чтобы повлиять на цвет крови.
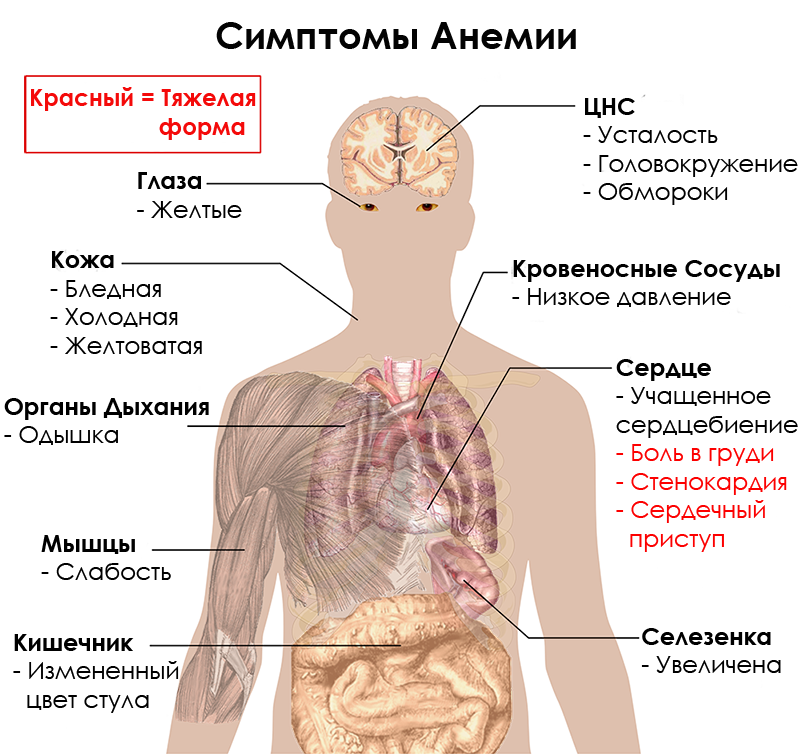
Цвет крови при анемии и цианозе
При анемии (недостаточном количестве гемоглобина или красных кровяных клеток), можно сказать, что кровь имеет более бледный красный цвет, хотя это видно лишь специалисту под микроскопом. Это потому, что когда гемоглобин не связан с кислородом, то эритроциты выглядят меньше по размеру и бледнее.
Когда кровь по причине проблем со здоровьем не переносит достаточно кислорода и его в ней мало, то это называют цианозом (синюхой). То есть, гемоглобин в крови есть, но он не связан с кислородом. Проявлением цианоза является приобретение кожей и слизистыми оболочками синюшного оттенка. Кровь при этом остается красной, но даже артериальная имеет цвет схожий с цветом венозной крови у здорового человека – с синим оттенком. Кожа, под которой проходят сосуды, что при нормальных условиях транспортируют кровь ярко алую богатую кислородом, внешне становится посиневшей.
Но при анемии симптомы цианоза могут быть даже не видны, потому что гемоглобина слишком мало, чтобы оказывать влияние на цвет кожи и слизистых оболочек, и они просто бледные. В этом случае внешне цианоз начнет проявляться только когда количество восстановленного (без кислорода) гемоглобина становится более половины от его общего количества.
Первая помощь и правила остановки артериального кровотечения
Оттого насколько быстро будет оказана первая помощь при артериальном кровотечении, будут зависеть и прогнозы здоровья пострадавшего. В первую очередь вызовите бригаду скорой помощи, а потом уже приступайте к самостоятельной остановке крови в месте повреждения. Существует несколько способов временного перекрытия наружного кровотечения из артерии:
- Пальцевое пережатие.
Поврежденную артерию сдавливают пальцами или кулаком, стараясь прекратить поток проходящей по ней крови. При данном способе остановки кровотечения, нужно зажимать определенные точки пульсации поврежденной артерии:
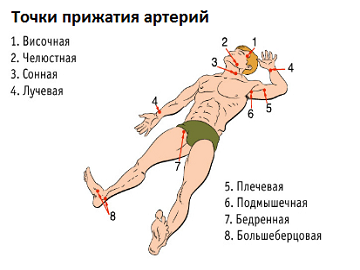
- прижатие сонной артерии осуществляется большим пальцем к позвоночнику сбоку от гортани;
- в случае раны в области ключицы, происходит прижатие подключичной артерии к первому ребру;
- при ране плеча нужно поднять конечность и произвести прижатие артерии к подмышечной ямке, данная точка прижатия поможет перекрыть кровоток при ранах локтя и кисти;
- при ранах ног осуществляется прижатие бедренной артерии в паху либо подколенной артерии в середине подколенной ямки.
Накладывание жгута.
После экстренного прижатия поврежденной артерии, необходимо продолжить временную остановку крови еще одним способом – с помощью жгута. Алгоритм действия при этом таков:
- поднять поврежденную конечность и в месте наложения жгута обернуть чистой тканью;
- обернуть и завязать жгут вокруг конечности (в качестве жгута подойдут ремни, пояса, шарфы, веревки);
- сделать пометку на ткани о времени пережатия жгутом.
По правилам, наложение жгута при артериальном кровотечении осуществляется на 2-3 сантиметра выше кровоточащей раны, при этом стоит учитывать, что жгут лишь временная мера. Зимой стягивать артерию жгутом возможно не больше часа, а в летнее время не более 2 часов.Тампонирование ранения.
Если артериальное кровотечение открылось в том месте, где жгут наложить невозможно, к примеру, на голове или шее, необходимо остановить кровь плотным тампоном из марлевой салфетки, бинта или ваты. Если возможно, смочите тампон перекисью водорода и сильно придавите им место кровоточащего сосуда. Данный способ остановки кровотечения подойдет также при ранении области голени и стопы, при этом стоит высоко поднять поврежденную конечность, что обеспечит отток крови.
 Первая помощь при артериальном кровотечении должна быть оказана с четкой последовательностью всех пунктов, поэтому стоит повторить алгоритм необходимых действий:
Первая помощь при артериальном кровотечении должна быть оказана с четкой последовательностью всех пунктов, поэтому стоит повторить алгоритм необходимых действий:
- незамедлительный вызов скорой помощи;
- пальцевое сдавливание поврежденной артерии;
- наложение жгута чуть выше области повреждения;
- тугое тампонирование раны.
Названные способы остановки крови являются временной доврачебной помощью и пациенту необходимо дальнейшее участие врачей. Однако если знать, как остановить артериальное кровотечение, то можно спасти человеку жизнь и облегчить его состояние до транспортировки в больницу. В клинических условиях пострадавшему смогут произвести перевязку сосуда либо ушьют рану. В некоторых случаях возможно протезирование поврежденного участка артерии.
Признаки кровотечения из артерии
Артериальная кровь с большой скоростью движется по организму под давлением кислорода, что создает большую опасность при повреждении артерии, так как кровь под напором будет вытекать гораздо быстрее, чем из поврежденной вены, где кровоток не усилен давлением. Обнаружить кровопотерю из артерии достаточно просто ведь признаки артериального кровотечения весьма характерны:
- цвет артериальной крови в месте повреждения ярко-алый;
- кровь жидкая и струится из раны значительным потоком;
- у пострадавшего происходит резкое снижение температуры тела;
- поток крови движется одновременно с ударами сердца, при этом пульсация в артериях, расположенных ниже повреждения, отсутствует либо нарушена;
- кровопотеря настолько сильная, что состояние человека ухудшается быстрыми темпами, появляется головокружение, слабость и при спазме сосудов возможна потеря сознания.
При травмировании любой артерии, человеку грозит смертельная опасность, но, в случае ранения крупных артерий, экстренная помощь понадобится в течение всего нескольких минут. Поэтому полезно знать, каковы признаки кровотечения из крупной артерии, и в каких случаях действовать нужно незамедлительно.
Главной отличительной чертой повреждения крупной артерии является то, что кровь имеет насыщенный красный цвет и хлещет из раны фонтаном. При этом оказание экстренной помощи человеку необходимо произвести в максимально быстрые сроки.
Определение уровня глюкозы
В некоторых случаях доктора назначают анализ крови на сахар, только не капиллярной (из пальца), а венозной. В этом случае биологический материал для исследования получают путём венепункции. Правила подготовки ничем не отличаются.
А вот норма глюкозы в венозной крови несколько отличается от капиллярной и не должна превышать 6,1 ммоль/л. Как правило, такой анализ назначают с целью раннего выявления сахарного диабета.
Венозная и артериальная кровь имеет кардинальные различия. Теперь вам вряд ли удастся спутать их, а вот определить некоторые расстройства с помощью вышеприведённого материала будет несложно.
Кровь в организме человека циркулирует в замкнутой системе. Основная функция биологической жидкости – обеспечение клеток кислородом и питательными веществами и вывод углекислого газа и продуктов обмена.
Как остановить венозное кровотечение
При небольшом повреждении вен конечностей бывает достаточно создать искусственный отток крови, подняв руку или ногу выше уровня сердца. На саму рану нужно наложить тугую повязку, чтобы максимально сократить кровопотерю.
Если повреждение глубокое, на место выше поврежденной вены нужно наложить жгут, чтобы ограничить количество крови, поступающей к месту повреждения. Летом его можно держать около 2 часов, зимой – на час, максимум полтора. За это время нужно успеть доставить пострадавшего в больницу. Если держать жгут дольше указанного времени, нарушится питание тканей, что грозит некрозом.
К месту вокруг раны желательно приложить лед. Это поможет замедлить кровообращение.
Функции артериальной крови
Артериальная кровь человека имеет ярко-алый цвет, обусловленную ее насыщением кислородом и содержанием в эритроцитах вещества оксигемоглобина. Она течет в артериях и капиллярах человека, ее движение по сосудам осуществляется под воздействием сердечных сокращений и сопротивления оболочки артерии. В свою очередь, ее объем оказывает на стенку артерии определенное давление, которое называется артериальным давлением и является одним из основных жизненных параметров человека.
Кровообращение выполняет несколько функций:
- перенос кислорода от легких к тканям и углекислого газа обратно от органов к легким;
- транспорт питательных веществ от желудочно-кишечного тракта к другим органам;
- перенос продуктов распада веществ к почкам, кишечнику, потовым железам, легким для выведения из организма;
- поддержание нормальной температуры тела с перемещением крови от более нагретых участков тела к менее нагретым;
- защита организма при помощи растворенных клеток иммунитета и свертывающей системы.
Кровь другого цвета у различных живых существ
Далеко не у всех живых организмов кровь красного цвета.
Белок придающий такой цвет у человека гемоглобин, содержащийся в гемоглобине. У других живых существ вместо гемоглобина иные жиросодержащие белки.
Наиболее распространенными оттенками помимо красного являются:
-
Голубой.
Таким цветом могут похвастаться ракообразные, пауки, моллюски, осьминоги и кальмары. И голубая кровь имеет огромное значение для этих существ, так как наполнена важными элементами. Вместо гемоглобина содержится гемоцианин, в котором содержится медь. -
Фиолетовый.
Этот цвет у морских беспозвоночных и некоторых моллюсков. Обычно такая кровь бывает не только фиолетовой, но и слегка розовой. Розового цвета кровь у молодых беспозвоночных организмов. В данном случае белок — гемэритрин. -
Зеленый.
Встречается у кольчатых червей и пиявок. Белок — хлорокруорин, близок к гемоглобину. Однако железо в этом случае не окисное, а закисное.
Как человеческое зрение воспринимает цвет вен
И так, почему вены синие далее предстоит узнать. Как известно световые волны бывают разные, соответственно, они имеют аналогичную длину. К самым длинным относятся красные, а самыми короткими являются фиолетовые, в пространстве между этими двумя видами находятся и остальные оттенки. Глаза начинают их отличать, когда волны попадают в поле зрения. Красные волны не очень сильно заметны под кожей, потому как находятся на расстоянии 5-10 миллиметров, также из-за своих размеров они не сильно выделяются. Еще одной причиной стал гемоглобин, который находится в крови, именно он поглощает красный цвет.
Почему вены синие на руках? Для того чтобы увидеть синий цвет достаточно посветить на руку обычным белым светом. При другом свете, к примеру синем, вены не будут видны, так как этот свет легко отражается и рассеивается, не попадая внутрь кожи. При белой, не загорелой коже синие вены особенно хорошо видны.










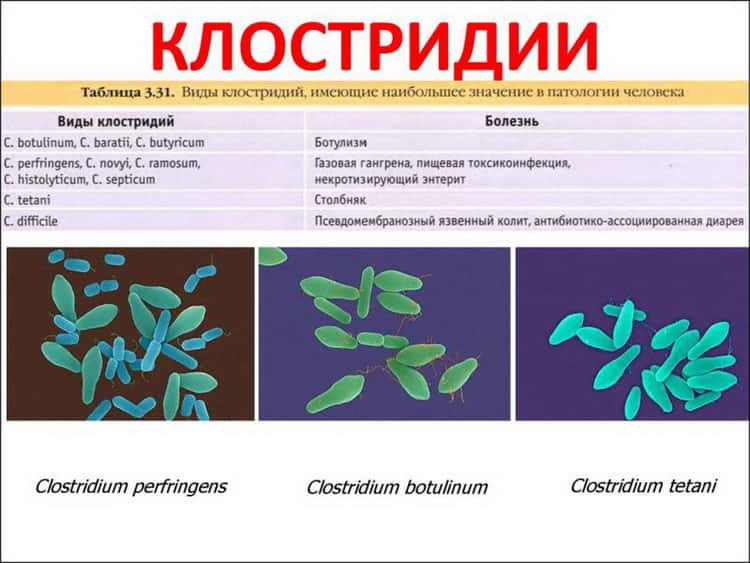
 Вредные микроорганизмы можно рассмотреть под микроскопом
Вредные микроорганизмы можно рассмотреть под микроскопом
 В род клостридий входит больше 100 видов, разделенных на 5 групп. Большинство этих микроорганизмов безобидно.
В род клостридий входит больше 100 видов, разделенных на 5 групп. Большинство этих микроорганизмов безобидно.

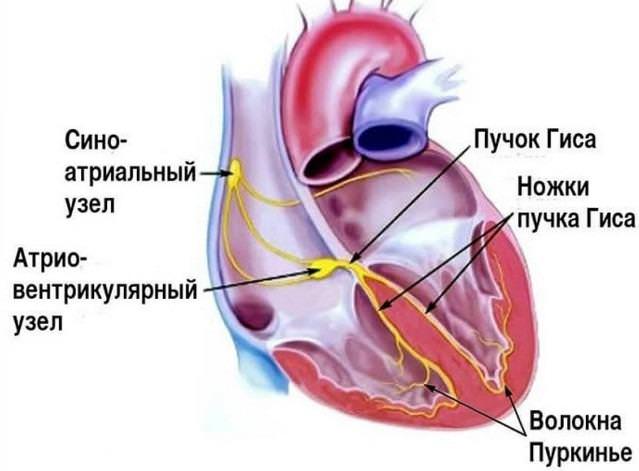
 У пациентов с СССУ может чередоваться редкий пульс с тахикардией.
У пациентов с СССУ может чередоваться редкий пульс с тахикардией.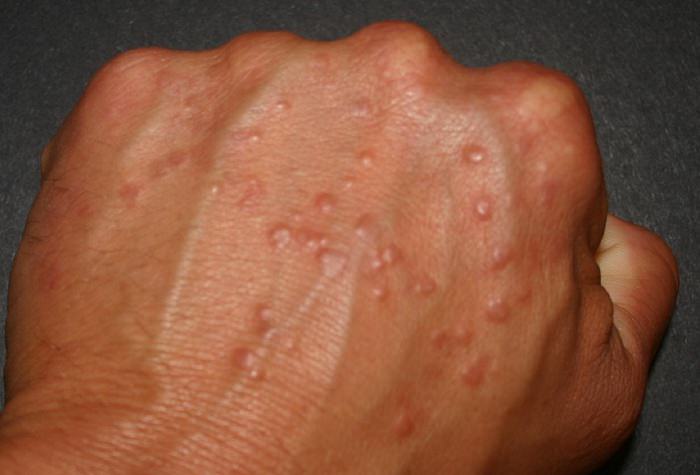
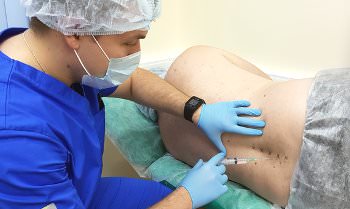
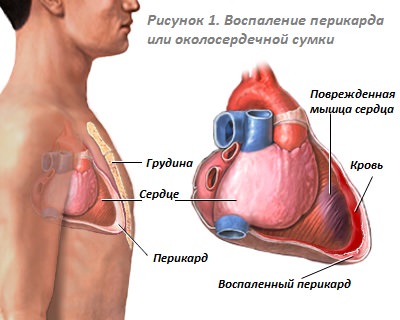
 В процессе воспаления, кровеносные сосуды растягиваются и теряют упругость. В разных случаях такого нарушения они могут сужаться и расширятся, и даже закрыться полностью.
В процессе воспаления, кровеносные сосуды растягиваются и теряют упругость. В разных случаях такого нарушения они могут сужаться и расширятся, и даже закрыться полностью. Поскольку данное заболевание может поражать разные органы, ему приписывается огромное количество симптомов, выявляемых в зависимости от локализации поражения.
Поскольку данное заболевание может поражать разные органы, ему приписывается огромное количество симптомов, выявляемых в зависимости от локализации поражения.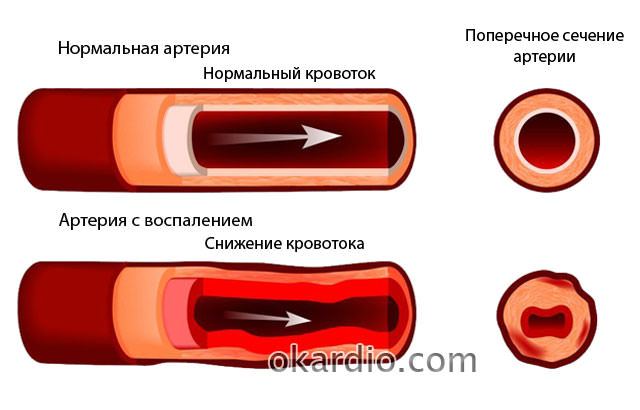 Васкулит сосуда
Васкулит сосуда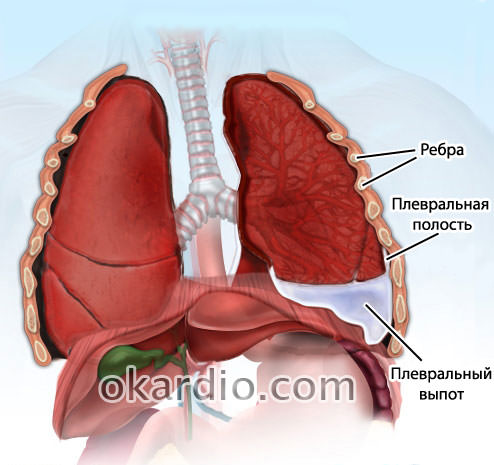 Плеврит
Плеврит

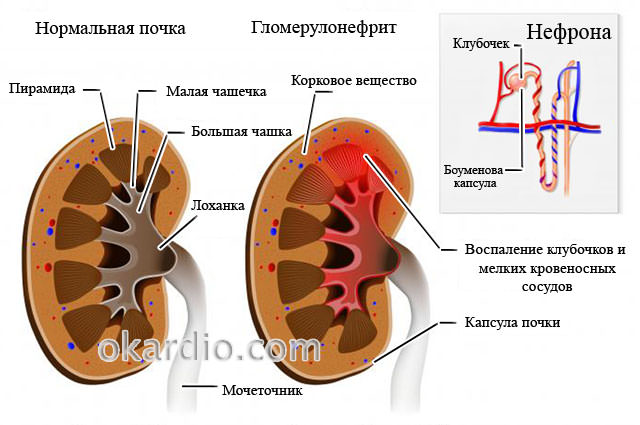 Гломерулонефрит. Нажмите на фото для увеличения
Гломерулонефрит. Нажмите на фото для увеличения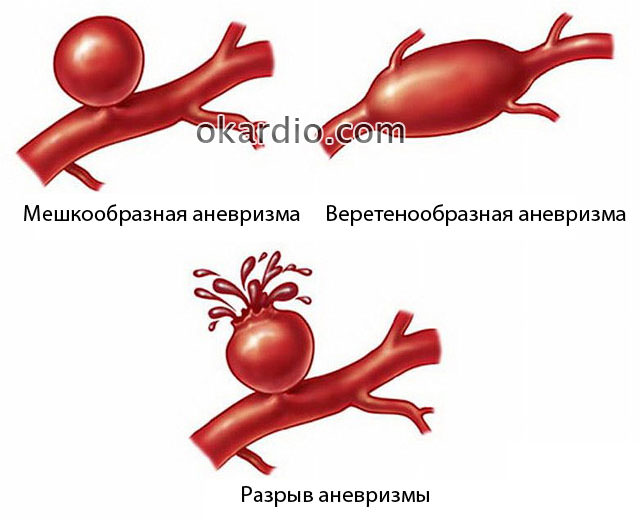 Типы аневризм
Типы аневризм Шприц Жане
Шприц Жане
 В12-дефицитная анемия относится к наиболее тяжелым формам малокровия. В тяжелых случаях приходится прибегать не только к инъекциям, но и к более радикальным средствам, включая переливание крови. Возникает эта болезнь чаще всего из-за неправильного питания, в котором ограничен или отсутствует витамин В12, а также из-за алкоголизма.
В12-дефицитная анемия относится к наиболее тяжелым формам малокровия. В тяжелых случаях приходится прибегать не только к инъекциям, но и к более радикальным средствам, включая переливание крови. Возникает эта болезнь чаще всего из-за неправильного питания, в котором ограничен или отсутствует витамин В12, а также из-за алкоголизма.