Активированные лимфоциты повышены или понижены
Дифференцировочные антигены Т-клеток
В процессе дифференцировки лимфоцитов на их поверхности появляются специфические мембранные молекулы гликопротеидов. Такие молекулы (антигены) можно обнаружить с помощью специфических моноклональных антител. Получены моноклональные антитела, которые реагируют лишь с одним антигеном клеточной мембраны. С помощью набора моноклональных антител можно идентифицировать субпопуляции лимфоцитов.
Имеются наборы антител к дифференцировочным антигенам лимфоцитов человека. Антитела составляют относительно немного групп (или «кластеров»), каждая из которых узнает один единственный белок клеточной поверхности.
Создана номенклатура дифференцировочных антигенов лейкоцитов человека, выявляемых моноклональными антителами. Эта CD-номенклатура (CD — cluster of differentiation — кластер дифференцировки) базируется на группах моноклональных антител, реагирующих с одними и теми же дифференцировочными антигенами.
Получены многоклональные антитела к ряду дифференцировочных антигенов Т-лимфоцитов человека. При определении общей популяции Т-клеток могут быть использованы моноклональные антитела специфичностей CD (CD2, CD3, CDS, CD6, CD7).
Известны дифференцировочные антигены Т-клеток, которые характерны либо для определенных стадий онтогенеза, либо для различающихся по функциональной активности субпопуляций. Так, CD1 — маркер ранней фазы созревания Т-клеток в вилочковой железе. В процессе дифференцировки тимоцитов на их поверхности экспрессируются одновременно маркеры CD4 и CD8. Однако в последующем маркер CD4 исчезает с части клеток и сохраняется только на субпопуляции, переставшей экспрессировать антиген CD8. Зрелые CD4+ клетки являются Тх. Антиген CD8 экспрессируется примерно на ⅓ периферических
Т-клеток, которые созревают из CD4+/CD8+ Т-лимфоцитов. Субпопуляция CD8+ Т-клеток включает цитотоксические и супрессорные Т-лимфоциты. Антитела к гликопротеинам CD4 и CD8 широко используются для того, чтобы различать и разделять Т-клетки соответственно на Тх и Тц.
Кроме дифференцировочных антигенов, известны специфические маркеры Т-лимфоцитов.
Т-клеточные рецепторы для антигенов представляют собой антителоподобные гетеродимеры, состоящие из полипептидных α- и β-цепей. Каждая из цепей имеет длину в 280 аминокислот, большая внеклеточная часть каждой цепи свернута в два Ig-подобных домена: один вариабельный (V) и один константный (С). Антителоподобный гетеродимер кодируется генами, которые собираются из нескольких генных сегментов в процессе развития Т-клеток в вилочковой железе.
Различают антигеннезависимую и антигензависимую дифференцировку и специализацию В — и Т-лимфоцитов.
Антигеннезависимая пролиферация и дифференцировка генетически запрограммированы на образование клеток, способных давать специфический тип иммунного ответа при встрече с конкретным антигеном благодаря появлению на плазмолемме лимфоцитов особых «рецепторов».
Она совершается в центральных органах иммунитета (тимус, костный мозг или фабрициева сумка у птиц) под влиянием специфических факторов, вырабатываемых клетками, формирующими микроокружение (ретикулярная строма или ретикулоэпителиальные клетки в тимусе).
Антигензависимая пролиферация и дифференцировка Т- и В-лимфоцитов происходят при встрече с антигенами в периферических лимфоидных органах, при этом образуются эффекторные клетки и клетки памяти (сохраняющие информацию о действовавшем антигене).
Образующиеся Т-лимфоциты составляют пул долгоживущих, рециркулирующих лимфоцитов, а В-лимфоциты — короткоживущих клеток.
Виды Т-лимфоцитов и их функции
Существует несколько видов Т-клеток:
- Эффекторы.
- Хелперы.
- Цитотоксические
- Регуляторные.
- Киллеры.
- Гамма-дельта.
- Памяти.
Т-хелперы помогают другим лейкоцитам в иммунологических процессах, в превращении В-лимфоцитов в плазматические клетки. Т-хелперы известны как CD4 Т-лимфоциты, поскольку имеют гликопротеин CD4 на мембране. Т-хелперы активируются, когда связываются с молекулярными антигенами ГКГ класса II, которые располагаются на поверхности антигенпрезентативных клеток. После активации Т-лимфоциты делятся и выделяют белки, называемые цитокинами, которые регулируют активный иммунный ответ. Клетки могут дифференцировать в один из нескольких подтипов лимфоцитов – TH1, TH2, TH3, TH17, TH9 или TFH. Т-лимфоциты этого вида могут быть представлены фенотипом CD3. Данные гликопротеиды (CD4 и CD3) помогают мобилизовать иммунную систему и уничтожить патогенный микроорганизм.
Цитотоксические Т-лимфоциты (ЦТЛ) уничтожают раковые или инфицированные вирусом клетки, участвуют в отторжении трансплантата. Известны как CD8 Т-клетки, поскольку имеют гликопротеин CD8 на мембране. Распознают мишени путем связывания с пептидными молекулами ГКГ класса I, которые присутствуют на мембране зародышевых клеток.
Регуляторные Т-лимфоциты играют ключевую роль в поддержании иммунологической толерантности. Их основная задача – вовремя отключить иммунную реакцию при уничтожении патогенного микроорганизма. Эту функцию совместно выполняют Т-киллеры и Т-хелперы.
Что такое T-лимфоциты, и где они образуются
Предшественники агранулоцитов появляются в костном мозге. В вилочковой железе происходит процесс созревания. Определенные гормоны и ткани на конечном этапе созревания оказывают влияние на дифференциацию лимфоцитов. Каждый тип Т-клеток отличается структурно и функционально друг от друга. Лимфоциты вырабатываются в костном мозге и в малых количествах в селезенке и лимфоузлах. При нарушениях в работе костного мозга или лейкозах различной этиологии увеличиваются лимфоузлы, что является первым признаком патологических состояний.
Т-клетки можно отличить от других лимфоцитов наличием специального рецептора на мембране. Большинство Т-лимфоцитов несут на мембране клеточный рецептор, состоящий из альфа- и бета-цепей. Такие лимфоциты принято называть альфа-β-Т-клетками. Они – часть приобретенной иммунной системы. Специализированные гамма-дельта-Т-клетки (менее распространенный тип Т-лимфоцитов в организме человека) имеют инвариантные Т-клеточные рецепторы с ограниченным разнообразием.
СD8 это Т-лимфоциты киллеры Тk, или цитотоксические лимфоциты CTL. Эти клетки также взаимодействуют с Аг, но для этого молекула СD8 на клеточной мембране Т-лимфоцита должна вступить во взаимодействие с HLA 1 класса.
Следует обратить внимание, что молекулы МНС-I способны по своим биохимическим свойствам связать пептидные фрагменты Аг в цитозоле клетки. Это могут быть белки, которые синтезировались внутри клетки, а могут быть белки вирусов, бактерий, гельминтов, простейших, которые инфицировали клетку
Тк способны действовать самостоятельно, без участия системы комплемента. Они распознают чужеродные Аг, синтезируемые или находящиеся внутри клетки, т.е. Аг любых вирусов и некоторых опухолевых клеток в комплексе с HLA 1 класса. Тк разрушают только те клетки-мишени, на мембране которых имеются Аг в связке с MHC-I. Механизм деструкции заключается в формировании пор, осмотическом лизисе и индукции апоптоза. Установлено, что один Тк способен лизировать несколько клеток мишеней со средней скоростью 4 клетки в час. Лизис осуществляется быстро и завершается в среднем за 1-3 часа. Процесс разрушения клеток мишеней протекает в 3 стадии: 1. Распознавание клеток мишеней и контакт с Тк – на это уходит не более 1 минуты. 2. Летальный удар – необратимая стадия, осуществляемая в среднем за 5 минут. 3. Гибель клетки мишени длится от нескольких минут до нескольких часов, но уже не требует присутствия Т-лимфоцита.
Существует несколько механизмов гибели клетки-мишени. Основной из них заключается в выделении CD8+ особых литических белков, получивших наименование перфорины и цитолизины. К цитолизинам, в частности, относится сериновые протеазы – гранзимы. И перфорины и цитолизины содержатся в лизосомах CTL. Попадают они в клетку-мишень (КМ) в стадии летального удара. Происходит это следующим образом. Перфорин и гранзимы покидают CTL по механизму экзоцитоза в сторону клетки-мишени. При этом молекулы перфорина встраиваются в мембрану КМ в форме мономера, а затем, полимеризуясь (проходя стадию полимеризации), образуют в ней поры. В сформированные перфорином отверстия в мембране в КМ проникают гранзимы. Кроме того, гранзимы способны поступать в КМ путём эндоцитоза.
Одним из механизмов, приводящих к гибели клетки-мишени под воздействием CTL, является запуск апопотоза. Благодаря взаимодействию так называемого Fas лиганда на CTL с молекулами Fas на клетке-мишени происходит активация цитоплазматических белков. Последние связываются с доменами смерти, вызывающими гибель клетки-мишени (см. 3.11.14).
Последующие процессы разрушения КМ под воздействием гранзимов и активации доменов смерти чрезвычайно сходны. В КМ происходит активация особых протеаз, подобных ферменту, разрушающих IL-1.
Недавно показано, что CTL содержат особый фермент, получивший название специфическая для Т-клеток протеиназа-1. Это сериновая протеиназа, также сконцентрированная в гранулах, способная разрушать мембрану клетки мишени.
Эффектор
Эффектор ( Effector) Небольшая молекула, связывающаяся с репрессором или ферментом и приводящая к их ингибированию или активации.
|
Коферменты и простетические группы, функционирующие как переносчики водорода, различных групп или электронов, и отношение их к витаминам. |
Эффекторы по своей структуре не имеют ничего общего с субстратами ферментов. Они стерически отличны от субстратов. Поэтому говорят об аллостерических эффекторах, а центры, ответственные за регуляцию, называют аллостерическими центрами ферментов.
Эффекторы — ингибиторы, управляющие активностью репрессоров. В случае образования индуцируемых белков-ферментов роль эффектора выполняет метаболит-индуктор, который инактивирует репрессор, ъ результате чего снимается репрессия гена-оператора. Соединение эффектора с рецрессором меняет сродство последнего к оператору. Такое взаимодействие эффекторов с репрессором создает условия для транскрипции на цистронах оперона соответствующей мРНК, а это в свою очередь вызывает синтез закодированных в этих цистронах белков-ферментов.
Центральные эффекторы могут осуществлять координированное движение, только пластически реагируя на совокупную сигнализацию с афферентационного поля, приспосабливая посылаемые импульсы к тому, что в текущей реальной ситуации имеет место на периферии ( с. Саккады, создавая афферентный поток, держат мозговые центры в курсе текущего события, в частности о положении глаза в орбите. Необходимость в оценке текущей реальной ситуации на периферии возникает и в связи с непрерывным изменением свойств мышц.
Любой эффектор, таким образом, связан элементами рефлекторной дуги с соответствующим рецептором и запускается в действие при раздражении данного рецептора. Ответная реакция организма возникает вследствие распространения по рефлекторной дуге возбуждения ( сигнала), появляющегося при раздражении рецептора.
Эффекторы аллостерических ферментов изменяют степень сиг-моидальиости графика зависимости v от
Такие эффекторы называют корепрессорами, а соответствующие ре-гуляторные белки — белками-репрессорами или апо реп рессорами. Синтез ферментов репрессибельного оперона включается посредством дере-прессии.
Индуктор ( эффектор) — молекула, способная вызывать синтез данного фермента с целью приспособления его к структуре субстрата.
Цитотоксины как неспенифнчные эффекторы обладают способностью нарушать структуры различных биологических мембран, изменяя тем самым клеточную проницаемость и. В отдельных случаях цитотоксины способны даже разрушать мембраны: растворять мембраны лейкоцитов, лимфоцитов, тромбоцитов, микрофагов кровн.
Цитотоксины как неспецифичные эффекторы обладают способностью нарушать структуры различных биологических мембран, изменяя тем самым клеточную проницаемость и направления внутриклеточных процессов. В отдельных случаях цитотоксины способны даже разрушать мембраны: растворять мембраны лейкоцитов, лимфоцитов, тромбоцитов, микрофагов крови.
Большое количество эффекторов свидетельствует о сложной регуляции образования микротрубочек в клетке. Ассоциация, видимо, начинается в одной точке клетки и идет в одном направлении при добавлении мономеров к удлиняющемуся или головному концу лолимера, тогда как на хвостовом конце преобладает диссоциация. Вероятно, сумма этих векторных процессов обусловливает наблюдаемый медленный аксональный поток тубулина.
|
Связывание субстрата с ферментом ( А и действие отрицательного ( Б и положительного ( В эффектора на каталитическую активность аллостери-ческого фермента. |
Если действие эффектора приводит к понижению каталитической активности фермента, такой эффектор называется отрицательным, или ингибитором. Положительным называют эффектор, действие которого повышает каталитическую активность фермента. Положительным эффектором, или активатором, чаще всего бывает субстрат данного фермента.
Нормальная функция иммунного эффектора и гомеоста-тическая регуляция иммунной реакции зависят от ряда растворимых продуктов, известных как цитокины, которые синтезируются и выделяются лимфоцитами и другими видами клеток. Цитокины оказывают плейотрогшый эффект на иммунную и воспалительную реакцию. Для иммунной реакции необходимо взаимодействие различных клеточных популяций — регуляция реакции на антитела, аккумуляция иммунных клеток и молекул в воспалительных участках, начало реакций острой фазы, контроль цитотоксичной функции макрофагов и многие другие процессы, важные для сопротивляемости хозяина. Они находятся под влиянием и даже в зависимости от цитокинов, действующих индивидуально или коллективно.
Нулевые лимфоциты
К ним относят лимфоциты, не имеющие T и B маркеров. Они составляют до 10% от всей популяции лимфоцитов. К ним относят NК-клетки (естественные киллеры) и K-клетки (киллерные).
Справочно. Основным отличием NK-клеток от T-киллеров является способность уничтожать не сенсибиллизированные клетки-мишени.
K-клетки отвечают за антителозависимую клеточную цитотоксичность. Они отражают взаимодействия гуморального и клеточного звеньев иммунитета, а также выступают в качестве «наводчиков» эффекторных (выполняющих функцию – в данном случае уничтожение) клеток на мишень.
NК- клетки обеспечивают контроль за качеством клеток и участвуют в формировании противовирусного иммунитета, обеспечиваютзащиту от роста опухолей и размножения мутировавших (дефектных) клеток.
Природа антигенспецифичного Т-клеточного рецептора
Молекулы, взаимодействующие с антигеном
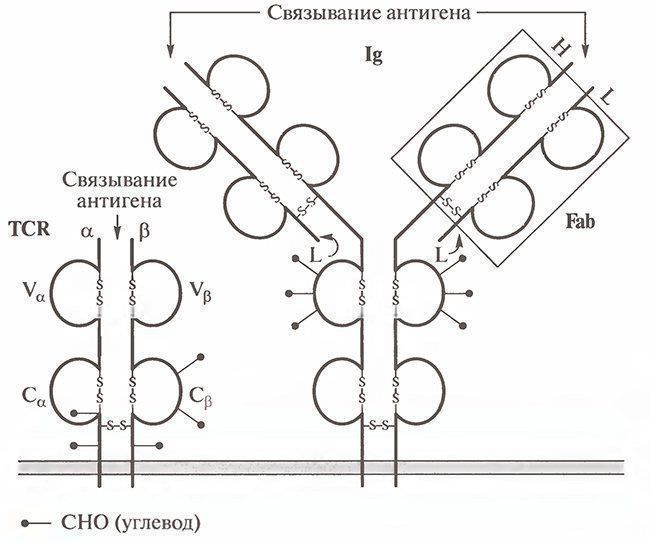 Рис. 8.1. Преобладающая форма антигенсвязывающих цепей TCR, α- и β-цепи и связанный с мембраной lg с указанным Fab-фрагментом
Рис. 8.1. Преобладающая форма антигенсвязывающих цепей TCR, α- и β-цепи и связанный с мембраной lg с указанным Fab-фрагментом
- Валентность и конформация. Т-клеточный рецептор является двухцепочечной структурой, формирующей один антигенсвязывающий центр. Таким образом, TCR является моновалентным и напоминает моновалентный Fab-фрагмент антитела. Обширные взаимодействия между доменами каждой цепи TCR придают его структуре устойчивую конформацию. Иммуноглобулин, напротив, является четырехцепочечной молекулой с шарнирной областью и двумя антигенсвязывающими центрами. Эти особенности придают молекуле lg гибкость, что позволяет ей бивалентно связываться с антигенами разных форм и размеров.
- Распознавание антигена. lg связывается с разными типами антигенов (углеводами, ДНК, липидами и белками), которые встречаются в жидкостях, например сыворотке. Мы также указали, что lg может реагировать на линейные и конформационные эпитопы в антигене. Таким образом, для того чтобы вызвать антительный ответ, необходимы определенная трехмерная структура и аминокислотная последовательность антигена.
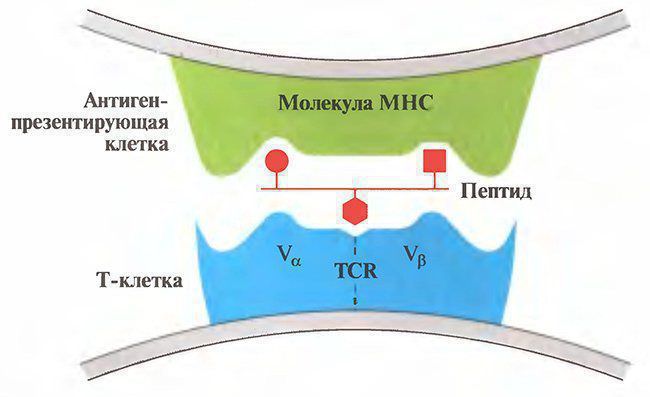 Рис. 8.2. Взаимодействие TCR с молекулярным комплексом МНС-пептид
Рис. 8.2. Взаимодействие TCR с молекулярным комплексом МНС-пептид
- Секреция рецептора. В отличие от lg TCR не существует в специфической секретируемой форме и не секретируется при активации Т-клеток. Активация Т-клеток приводит к секреции цитокинов и/ или киллингу инфицированных клеток организма. Напротив, после того как антиген связывается с мембранным Ig и активирует В-клетку, В-клетка дифференцируется в плазматическую клетку и секретирует Ig с той же антигенной специфичностью, что была характерна для В-клетки, которая первоначально связала антиген.
- Отсутствие изменений в TCR во время ответа на антиген. В период ответа на антиген молекулы Ig подвергаются соматическому гипермутагенезу (что связано с созреванием аффинности) и переключению класса, связывающему один из генных наборов, кодирующих определенную V-область, с разными генами С-области. Эти механизмы являются уникальными для В-клеток: TCR не изменяются в период ответа на антиген.
Корецепторные молекулы
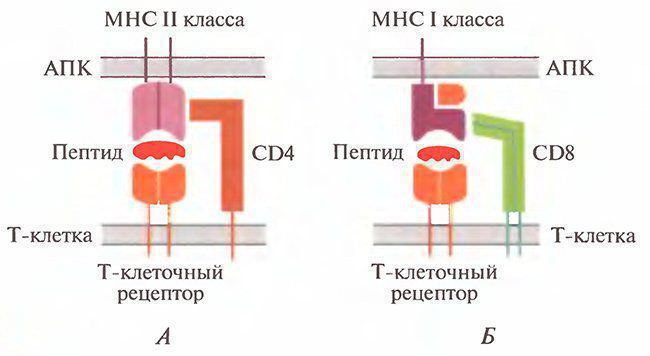 Рис. 8.3. Рецепторы TCR и их взаимодействие с молекулами МНС. (A) CD4 и (Б) CD8. Обозначены все молекулы
Рис. 8.3. Рецепторы TCR и их взаимодействие с молекулами МНС. (A) CD4 и (Б) CD8. Обозначены все молекулы
- Внеклеточные части CD4 и CD8 связываются с молекулами МНС на поверхности клетки, представляющей антиген для Т-лимфоцита — АПК. Молекула CD4 избирательно связывается с МНС II класса, a CD8 — с МНС I класса. На рис. 8.3 показано, что СЭ4+-Т-клетки взаимодействуют с клетками организма, экспрессирующими пептид, ассоциированный с МНС II класса, а С08+-Т-клетки — с клетками, экспрессирующими пептид, ассоциированный с МНС I класса. Это формирует основу для рестрикции (ограничения) Т-клеточного ответа по МНС.
- Связывание CD4 или CD8 с молекулами МНС, экспрессируемыми на АПК, способствует усилению связи Т-клеток с АПК. Таким образом, CD4 и CD8 действуют как молекулы адгезии при взаимодействии Т-клеток с АПК.
- Молекулы CD4 и CD8 вовлекаются в передачу сигнала после связывания антигена с TCR. Их внутриклеточные части специфически связаны с ферментами, известными как белковые тирозинкиназы, которые являются важными компонентами в процессе ранней активации Т-клеток.
- Уникальным свойством молекулы CD4 является то, что с ней связывается ВИЧ. Это позволяет вирусу инфицировать клетки, экспрессирующие CD4, что в последующем приводит к развитию СПИДа.
Комплекс Т-клеточного рецептора
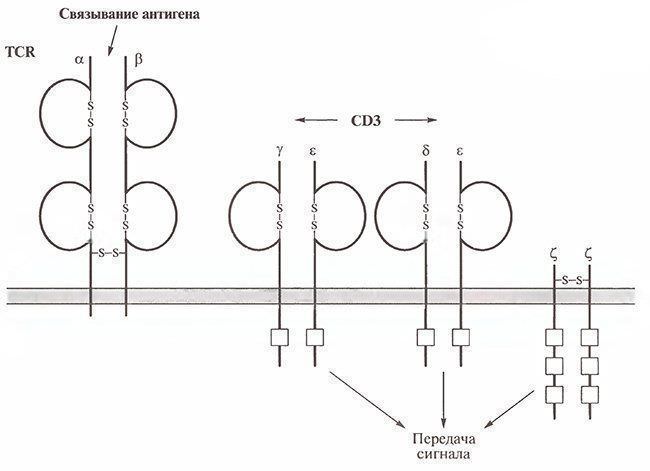 Рис. 8.4. Комплекс TCR. Т-клеточный рецептор и ассоциированный комплекс CD3 (γ-, δ- и ε-цепи), передающий сигнал, плюс ζ. Незакрашенные квадратики — ITAM
Рис. 8.4. Комплекс TCR. Т-клеточный рецептор и ассоциированный комплекс CD3 (γ-, δ- и ε-цепи), передающий сигнал, плюс ζ. Незакрашенные квадратики — ITAM
Интерпретация результатов анализов
Общее содержание лимфоцитов в крови
Чрезмерное повышение уровня лимфоцитов (CD3+ Т-клеток) в крови может указывать на инфекционные или воспалительные процессы. Такое состояние наблюдается при хронических лейкозах или бактериальных инфекциях. Снижение абсолютного числа Т-клеток указывает на дефицит клеточно-эффекторного иммунитета. Пониженное количество Т-лимфоцитов наблюдается при злокачественных новообразованиях, сердечном приступе, применении цитостатических препаратов или травмах различной этиологии.
В-клетки
Повышенные показатели В-лимфоцитов (CD19+ Т-клетки) наблюдаются при аутоиммунных заболеваниях, болезнях печени, бронхиальной астме, грибковых или бактериальных инфекциях. Хронический лимфолейкоз может стать причиной повышенного содержания В-лимфоцитов в кровеносном русле. Пониженные показатели В-лимфоцитов появляются при доброкачественных новообразованиях, агаммаглобулинемии или после удаления селезенки.
Т-хелперы
Если повышаются показатели абсолютного и относительного содержания Т-клеток с фенотипом СД3+CД4 (Т-хелперов), то это указывает на наличие аутоиммунных заболеваний, аллергических реакций или инфекционных болезней. Если чрезмерно понижаются показатели содержания Т-клеток в крови, то это признак ВИЧ, пневмонии, злокачественных новообразований или лейкоза.
ЦТЛ
Показатели ЦТЛ с фенотипом CD3+ CD8 повышаются при вирусных, паразитарных, бактериальных или аллергических патологиях. Нередко высокий показатель данного типа агранулоцитов является признаком ВИЧ. Снижение числа ЦТЛ с фенотипом CD8 свидетельствует о наличии аутоиммунной болезни, гепатита различной этиологии или гриппа. Исследуют соотношение CD4+/CD8 для оценки эффективности лекарственной терапии или мониторинга состояния здоровья ВИЧ-инфицированных.
Естественные (N) киллеры
Снижение общего количества натуральных киллеров с фенотипом CD16 ведет к развитию онкологических, вирусных, аутоиммунных заболеваний. Повышение приводит к отторжению трансплантата и осложнениям различной этиологии.
Т-хелперы
Справочно. Функция хелперов осуществляется за счёт синтеза цитокинов (информационных молекул, регулирующих взаимодействие между клетками).
В зависимости от продуцируемого цитокина, их разделяют на:
- T-хелперные клетки 1-го класса (продуцируют интерлейкин-2 и гамма-интерферон, обеспечивая гуморальный иммунный ответ на вирусы, бактерии, опухоли и трансплантанты).
- T-хелперные клетки 2-го класса (секретируют интерлейкины-4,-5,-10,-13 и отвечают за образование IgЕ, а также иммунного ответа, направленного на внеклеточные бактерии).
Т-хелперы 1-го и 2-го типа всегда взаимодействуют антагонистически, то есть повышенная активность первого типа угнетает функцию второго типа и наоборот.
Работа хелперов обеспечивает взаимодействие между всеми клетками иммунитета, определяя какой тип иммунного ответа будет преобладать (клеточный либо гуморальный).
Важно. Нарушение работы клеток-помощников, а именно недостаточность их функции, наблюдается у больных с приобретённым иммунодефицитом
Т-хелперы являются основной мишенью ВИЧ. В результате их гибели нарушается иммунная реакция организма на стимуляцию антигенов, что приводит к развитию тяжёлых инфекций, росту онкологических новообразований и летальному исходу.
Лимфоциты в крови
 |
Лимфоциты обладают удивительной способностью различать в организме «свое» и «чужое» вследствие наличия в их оболочке специфических участков — рецепторов, активирующихся при контакте с чужеродными белками. Лимфоциты осуществляют синтез защитных антител, лизис чужеродных клеток, обеспечивают реакцию отторжения трансплантата, иммунную память (способность отвечать усиленной реакцией на повторную встречу с чужеродным антигеном), уничтожение собственных мутантных клеток и др.
Каждая из перечисленных функций осуществляется специализированными формами лимфоцитов. Все лимфоциты делятся на три группы: Т-лимфоциты (тимусзависимые), В-лимфоциты (бурсазависимые) и нулевые.
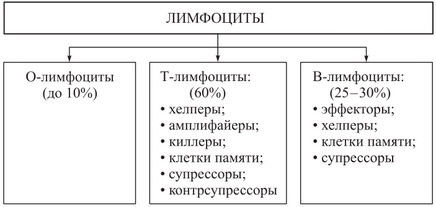
Рис. Характеристика лимфоцитов
Т-лимфоциты
Т-лимфоциты образуются в красном костном мозге из клеток- предшественников, проходят дифференцирование в вилочковой железе и затем расселяются в лимфатических узлах, селезенке или циркулируют в крови, где на их долю приходится 40-70% всех лимфоцитов.
Различают несколько форм Г-лимфоцитов, каждая из которых выполняет определенную функцию: клетки-хелперы (помощники) взаимодействуют с В-лимфоцитами, превращая их в плазматические клетки; клетки-супрессоры (угнетатели) блокируют чрезмерные реакции В-лимфоцитов и поддерживают постоянное соотношение разных форм лимфоцитов; клетки-киллеры (убийцы) непосредственно осуществляют реакции клеточного иммунитета, взаимодействуя с чужеродными клетками и разрушая опухолевые клетки, клетки чужеродных трансплантатов, клетки-мутанты, что сохраняет генетический гомеостаз.
Т-лимфоциты играют ведущую роль в иммунном надзоре. При ослаблении их функций возрастает опасность развития опухолей, аутоиммунных заболеваний (когда собственные ткани организма воспринимаются как чужие), повышается склонность к разным инфекциям.
В-лимфоциты
В-лимфоциты образуются в красном костном мозге, но у млекопитающих проходят дифференцирование в лимфоидной ткани кишечника, червеобразного отростка, нёбных и глоточных миндалин. В крови на их долю приходится 20-30% циркулирующих лимфоцитов. Основная функция В-лимфоцитов — создание гуморального иммунитета путем выработки антител. После встречи с антигеном В-лимфоциты мигрируют в костный мозг, селезенку и лимфатические узлы, где размножаются и трансформируются в плазматические клетки, которые являются продуцентами антител — иммунных у-глобулинов.
В-лимфоциты очень специфичны: каждая группа (клон) реагирует лишь с одним антигеном и отвечает за выработку антител только против него. Среди В-лимфоцитов тоже существует специализация.
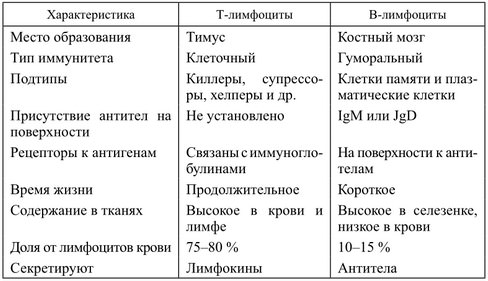
Таблица. Сравнительная характеристика Т- и В-лимфоцитов
Нулевые лимфоциты
Нулевые лимфоциты не проходят дифференцирования в органах иммунной системы, но при необходимости способны превратиться в В- или Т-лимфоциты. На их долю приходится 10-20% лимфоцитов крови.
Лимфоциты обеспечивают целостность организма не только путем защиты его от чужеродных агентов. Эти клетки несут макромолекулы с информацией, необходимой для управления генетическим аппаратом других клеток организма
Это имеет важное значение в процессах роста, дифференцировки, регенерации
Медицина
Нормальные значения Т-лимфоцитов в анализе крови
Нормальные показатели лимфоцитов различаются у разных возрастных групп. Связано с индивидуальными особенностями иммунной системы. Объем вилочковой железы, в которой находится основная часть агранулоцитов, в процессе старения уменьшается. До шестилетнего возраста в кровеносном русле преобладают лимфоциты, а с 6 лет – нейтрофилы.
Процентное соотношение количества Т-лимфоцитов в крови у разных возрастных групп:
- У новорожденных показатель составляет 14-36% от общего числа лейкоцитов.
- У грудных детей варьируется в пределах 41-78%.
- У детей от 12 месяцев до 15 лет постепенно снижается до 23-50%.
- У взрослых варьируется в диапазоне 18-36%.
Анализ количества Т-лимфоцитов является частным случаем общеклинического исследования крови. Данное исследование позволяет определить относительное и абсолютное содержание лимфоцитов в кровеносном русле. Иммунологическое исследование (иммунограмму) проводят для выявления концентрации лимфоцитов. Иммунограмма отображает показатели В и Т-клеток. Нормой Т-лимфоцитов принято считать 48-68%, а В-клеток – 4-18%. Соотношение Т-хелперов и Т-киллеров не должно в норме превышать 2.0.
 Иммунологическое исследование крови (иммунограмма)
Иммунологическое исследование крови (иммунограмма)

Comments
(0 Comments)