Врожденный порок сердца у детей симптомы, физиолечение
Врожденный порок сердца у новорожденных
У всех новорожденных первичные клинические проявления пороков позволяют судить о том, что нарушение в гемодинамике или в анатомическом распределении кругов кровообращения являются врожденными, то есть развились в процессе органогенеза. Потому зачастую причины порока сердца у новорожденных связаны с интоксикацией, генетическими отклонениями, нарушениями в дифференциации тканей.
В течении врожденного порока сердца у новорожденного выделяют три фазы:
- I фаза (адаптация): в организме ребенка происходит процесс адаптации и компенсации к гемодинамическим нарушениям, вызываемых пороком сердца, при тяжелых нарушениях кровообращения наблюдается значительная гиперфункция сердечной мышцы, переходящая в декомпенсацию;
- II фаза (компенсация): наступает временная компенсация, которая характеризуется улучшениями со стороны моторных функций и физического состояния ребенка;
- III фаза (терминальная): развивается при исчерпывании компенсаторных резервов миокарда и развитии дегенеративных, склеротических и дистрофических изменений в структуре сердца и паренхиматозных органов.
Причины развития патологии могут быть различны, поэтому даже полностью здоровые женщины, ведущие правильный образ жизни, в результате сталкиваются с тем, что их дети рождаются с проблемами сердца. Источники болезни:
- аборты, выкидыши и мертворожденные дети в анамнезе матери, причем связано это в основном с психологическим состоянием женщины, для которой беременность ассоциируются с сильнейшими отрицательными эмоциями;
- также причиной могут быть скрытые инфекции, оказавшие влияние на формирование эмбриона еще на ранних этапах развития;
- прием серьезных препаратов для лечения болезней во время беременности может привести к тому, что дети могут родиться с пороком;
- у сердечных патологий, в первую очередь, наследственная природа, поэтому если у кровных родственников имеются подобные заболевания, риск возникновения болезни;
- возрастает у каждого следующего младенца;
- закладка порока сердца, как правило, происходит на 3-8 неделе после зачатия, поскольку именно в этот период у эмбриона формируется сердце и сосудистое соединение, повлиять на которое способно вирусное заболевание, которое перенесла в этот период мама, причем наиболее опасными являются вирусы герпеса, краснухи, прием гормональных препаратов, анальгетиков и других серьезных медикаментов; возраст матери более 35 лет;
- неблагоприятная экология.
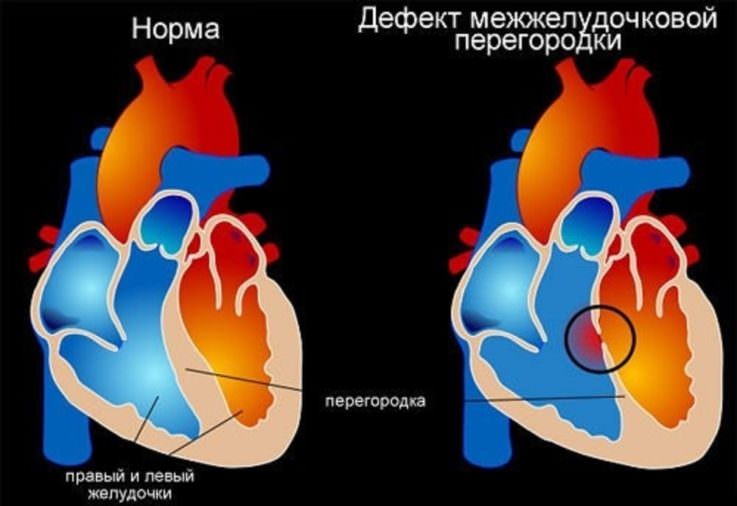
Дефект межжелудочковой перегородки
ДМЖП — это врождённый порок сердца, при котором между правым и левым желудочками сердца отмечается наличие дефекта.
В межжелудочковой перегородке выделяют три отдела: верхняя часть (мембранозная), средняя (мышечная) и нижняя (трабекулярная). Соответственно им называют и аномалии. По размерам они подразделяются на большие, средние и малые. Для правильности оценки величины их размер сравнивают с диаметром аорты. Небольшие дефекты (размером 1 — 2 мм), располагающиеся в мышечной части перегородки, называют болезнью Толочинова — Роже. Согласно выраженной аускультативной картине и отсутствию гемодинамических нарушений для их характеристики применяют выражение: «Много шума из ничего».
Внутрисердечные нарушения гемодинамики формируются у ребёнка через некоторое время после его рождения, как правило, на третьи-пятые сутки. Во время раннего неонатального периода, то есть в первые дни жизни ребёнка, шума в сердце может не быть. Постепенное снижение давления в правом желудочке и в системе лёгочной артерии создаёт разницу между давлениями в желудочках, в результате чего возникает сброс слева направо. Дополнительный объём крови, который поступает в лёгочную артерию и правый желудочек сердца, приводит к перенаполнению сосудов малого круга кровообращения, вследствие этого развивается повышение давления в сосудах лёгких (так называемая лёгочная гипертензия).
Клинически ДМЖП проявляется синдромом сердечной недостаточности, которая в зависимости от размеров дефекта развивается, как правило, на первом-третьем месяцах жизни. В результате кровяного застоя в малом круге кровообращения могут развиваться ранние и тяжёлые пневмонии. Во время осмотра ребёнка можно выявить учащённое сердцебиение и одышку, расширение границ сердца, а также перемещение верхушечного толчка (он проявляется пульсацией при прощупывании в области верхушки сердца) влево и вниз. В некоторых случаях определяется так называемый симптом «кошачьего мурлыканья» (вибрация (или дрожание) грудной стенки, которое напоминает мурлыканье кошки при её поглаживании). Как правило, определяется систолический шум, он достаточно интенсивный и выслушивается над всей областью сердца. При прощупывании живота определяется увеличение размеров печени и селезёнки.
В развитии лёгочной гипертензии выделяют три стадии:
- гиперволемическая (застой крови, который приводит к отёку лёгких и частому присоединению инфекции, в результате чего развиваются пневмонии, проявляющиеся в ранние сроки жизни, имеющие тяжёлое течение и плохо поддающиеся лечению);
- переходная стадия, когда ребёнок перестаёт болеть, начинает прибавлять в весе и становится более активным; стабильное состояние в эту фазу является наилучшим периодом для проведения хирургического лечения;
- так называемая высокая лёгочная гипертензия возникает в том случае, когда оперативная коррекция не была проведена, у этого процесса нет обратного развития, и он в основном приводит к сильному увеличению давления в лёгочной артерии. Самым характерным признаком этой стадии является поэтапное нарастание цианоза (вначале периферического, а потом и общего); это происходит из-за сброса крови через дефект в перегородке справа налево. Наличие у пациентов третьей стадии зачастую становится основной причиной отказа врачей кардиохирургов от оперативного вмешательства.
Наиболее информативными методами выявления данной патологии являются электрокардиография и эхокардиография (ультразвуковое исследование сердца, ЭхоКГ).
Лечение дефекта межжелудочковой перегородки сердца совокупно включает в себя консервативную (медикаментозную) терапию сердечной недостаточности и оперативную коррекцию порока. Хирургические вмешательства делятся на паллиативные (облегчающие течение заболевания — операция суживания лёгочной артерии) и радикальные (пластика дефекта заплатой в условиях искусственного кровообращения и низкой температуры).
Тетрада Фалло
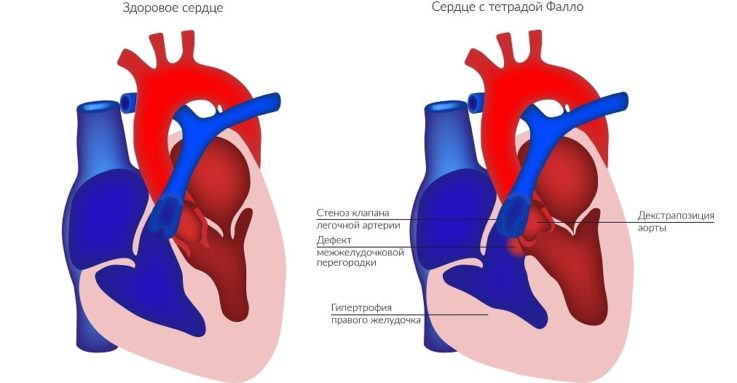
Тетрада Фалло – это сочетанная врождённая аномалия сердца, которая включает в себя четыре порока:
- дефект межжелудочковой перегородки;
- стеноз выходного отдела правого желудочка;
- декстропозиция аорты (когда она отходит частично от правого желудочка или кровоток преимущественно в ней поддерживается за счёт работы левого желудочка);
- гипертрофия миокарда правого желудочка (разрастание его мышечного компонента развивается с возрастом).
В зависимости от времени появления цианоза выделяют пять клинических форм и соответственно столько же периодов клинического проявления порока:
- ранняя цианотичная форма (появление синюшной окраски с первых месяцев или первого года жизни);
- классическая (на втором-третьем году жизни);
- тяжёлая (протекает с приступами одышки и цианоза);
- поздняя цианотичная (возникновение синюшности к 6 – 10 годам);
- ацианотичная (бледная) форма.
Синюшное окрашивание губ и кожного покрова при тяжёлой форме тетрады Фалло появляется с трёх-четырёх месяцев жизни ребёнка и становится стабильно выраженным примерно к году. Оно может усиливаться при плаче, кормлении, натуживании или эмоциональном напряжении. Любая физическая активность (подвижная игра, ходьба, бег) сопровождается быстрым появлением слабости, одышки, учащённого сердцебиения, головокружения. После нагрузки пациенты с данной патологией принимают характерное положение сидя на корточках.
Крайне тяжёлым проявлением данной патологии служат приступы, которые обычно появляются в возрасте 2 — 5 лет. Они развиваются внезапно, сопровождаясь при этом беспокойством ребёнка, учащённым сердцебиением, резкой слабостью, усилением одышки и цианоза и даже потерей сознания. Возможно развитие остановок дыхания, а также судорог.
Дети с тетрадой Фалло отстают в физическом развитии (у них наблюдается гипотрофия II — III степени), они часто заболевают острыми респираторными заболеваниями, хроническим тонзиллитом и гайморитом, повторяющимися пневмониями. У взрослых пациентов с таким пороком сердца возможно присоединение туберкулёза легких.
Оперативное лечение включает в себя два этапа
Первый этап. До трёх лет проводятся операции, которые существенно облегчают жизнь больных с данным пороком. Цель их выполнения состоит в увеличении притока крови к малому кругу кровообращения.
Второй этап. Проводится через пару месяцев после первого. Операция радикальная и осуществляется в условиях искусственного кровообращения с применением остановки и охлаждения сердца. Общее снижение температуры до 21,6 градусов. После пережатия аорты вскрывается полость правого желудочка и под контролем зрения выполняют хирургические приёмы по устранению сужения его выходного отдела. Дефект межжелудочковой перегородки устраняют при помощи подшивания заплаты П-образными швами. Затем вшивают заплату в переднюю поверхность правого желудочка с целью расширения выходного отдела.
Течение порока значительно зависит от степени лёгочного сужения. Примерно 25% детей, имеющих тяжёлую форму тетрады Фалло, погибают на первом году жизни, половина из них — в периоде новорождённости. Средняя продолжительность жизни без операции примерно двенадцать лет, менее пяти процентов больных доживают до сорокалетия. Причиной смерти больных с данной аномалией развития чаще всего становится ишемический инсульт вследствие тромбоза сосудов головного мозга.
Отдалённые результаты хирургической коррекции порока вполне благоприятные: пациенты хорошо переносят физические нагрузки, социально активны и трудоспособны. Но чем в более позднем возрасте проведена операция, соответственно тем хуже и её отдалённые результаты. Абсолютно все пациенты с этим пороком нуждаются в динамическом наблюдении врачей кардиолога и кардиохирурга, профилактическом назначении антибиотиков перед проведением любых хирургических или стоматологических процедур, которые имеют потенциальную опасность в отношении развития бактериальной инфекции.
Диагностика ВПС
Данные осмотра помогают оценить цвет кожи, наличие бледности, синюшности, аускультация выявляет шум в сердце, ослабление, расщепление или усиление тонов.

Инструментальное исследование при подозрении на врожденный сердечный порок включает:
- рентген-диагностику органов грудной полости;
- ЭКГ;
- эхологическое исследование;
- фоно-КГ;
- ангио-КГ;
- зондирование сердца.
ЭКГ – признаки: гипертрофия различных частей, аномалии проводимости, нарушенный ритм. При помощи суточного мониторинга выявляют скрытые аритмии. Фонокардиографией подтверждают наличие патологических сердечных тонов, шума.
По рентгенограмме исследуют легочной рисунок, расположение сердца, очертания и размер.
Эхологическое исследование помогает определить анатомические отклонения клапанного аппарата, перегородок, позицию крупных сосудов, двигательную способность миокарда.
Виды ВПС
Такое заболевание, как ВПС, встречается преимущественно у новорождённых и детей, но и не исключается развитие врождённого порока сердца и у взрослых. Если ребёнок, преодолел возрастной барьер в 15 лет с данным видом заболевания, то — это не говорит о том, что смертельная опасность минула. Человек, будучи в возрасте с наличием недуга ВПС, в любую минуту может умереть, что напрямую зависит от типа и характера этого недуга. Рассмотрим, какие виды врождённого сердечного порока известны и встречаются чаще всего.
В медицине известны около ста видов различных пороков сердечной мышцы. Конечно же, рассматривать все виды мы не будем, а выделим только основные из них. ВПС подразделяют на два вида: синие и белые. Это подразделение основано, в первую очередь, на интенсивности изменения окраса кожных покровов.
«Белый» вид ВПС, в свою очередь, подразделяется на 4 группы, которые называются:
- Обогащённый малый круг кровообращения. Причиной формирования которого являются: артериальный проток, дефект межпредсердной перегородки и дефект межжелудочковой перегородки.
- Обеднённый малый круг. При этом наблюдаются признаки изолированного стеноза.
- Обеднённый большой круг. (Аортальный стеноз, коарктация аорты).
- Без наличия изменений гемодинамики: сердечные диспозиции и дистопии.
«Синий» вид врождённого порока сердца включает в себя 2 группы:
- С обогащением малого круга кровообращения, которому характерна полная транспозиция магистральных сосудов.
- Преимущественно обеднённый малый круг. (Аномалии Эбштейна).
Дефект межжелудочковой перегородки — это вид врождённого порока сердца, диагностирующийся у новорождённых в достаточно частых случаях. Характеризуется дефект межжелудочковой перегородки тем, что происходит смешивание обогащённой крови с необогащенной. При этом виде заболевания в сердце появляется отверстие, которое и представляет собой дефект. Это отверстие формируется на границе между правым и левым желудочками. Через отверстие происходит перемещение обогащённой крови из левого желудочка в правый, где и осуществляется её смешивание с необогащенной.
Если дефект имеет незначительный размер, то, у ребёнка признаки заболевания могут не проявляться. В случае значительного размера отверстия наблюдается активное смешивание крови, что проявляется в виде посинения кожных покровов на губах и пальцах.
Дефект межжелудочковой перегородки поддаётся лечению, поэтому в частых случаях удаётся спасти ребёнка. Если отверстие между желудочками имеют незначительные размеры, то, с течением времени оно может самостоятельно зарасти. При повышенном размере отверстия потребуется хирургическое вмешательство. Но все же стоит заметить, если этот вид заболевания никак не проявляется, то, какое-либо воздействие или вмешательство осуществлять не рекомендуется.
Двустворчатый аортальный клапан — вид ВПС, который также диагностируется у детей, но преимущественно в старшем возрасте. Заболевание характеризуется тем, что в клапане аорты образуется не три створки, как должно быть по анатомии, а только две, откуда и название вида заболевания — двустворчатый аортальный клапан. Посредством трехстворчатого клапана обеспечивается нормальный приток крови к сердцу. Формируется двустворчатый аортальный клапан преимущественно ещё во время нахождения плода в утробе матери на восьмой неделе беременности. Именно в это время происходит формирование сердечной мышцы, и если беременная мать в этот период будет нагружать себя физически или морально, то — это может повлиять на формирование врождённого порока сердца.
Двустворчатый аортальный клапан также поддаётся лечению, но хирургическое вмешательство осуществляется только в случае появления симптомов недуга или же если сердце испытывает сильные нагрузки.
Дефект межпредсердной перегородки — представляет собой отверстие, располагающееся между правым и левым предсердием. Возникает этот вид недуга у детей в довольно редких случаях, но его наличие приводит к беспокойству родителей. На самом деле, если отверстие незначительного размера, то оно может зарасти самостоятельно в течение неопределённого времени. Если же отверстие значительных размеров, тогда исправить ситуацию можно лишь путём хирургического вмешательства. Если этого не сделать, то этот вид ВПС приведёт к развитию сердечной недостаточности.
Приобретенные пороки
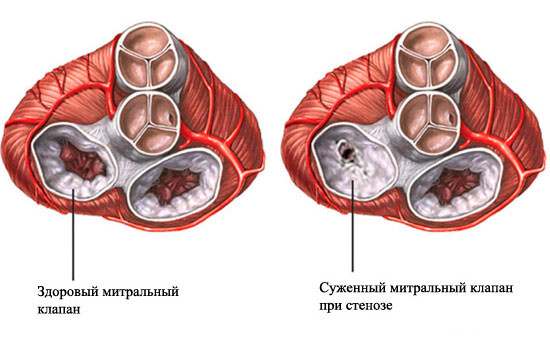
Приобретенные пороки сердца – это аномалии строения и функционирования клапанов сердца, появившиеся не внутриутробно, а в процессе жизни, под воздействием морфологических и функциональных изменений в работе сердца. В отличие от врожденного порока порок сердца приобретенный возникает вследствие инфекционного поражения или воспаления сердца, а также перегрузки камер сердца.
Приобретенный порок еще называют порок клапана сердца. Он проявляется в виде стеноза или недостаточности клапана, а иногда – как комбинированный порок сердца. Если поставлен диагноз порок, митральный клапан сердца не может регулировать ток крови, способствуя застою в большом и малом кругах кровообращения.
Перегрузка определенных отделов сердца вызывает их гипертрофию, что изменяет конфигурацию тени сердца. Если диагностика врожденных пороков сердца часто проводится уже на первом году жизни малыша, то пороки сердца у взрослых редко диагностируют своевременно.
Пороки развития сердца классифицируются по разным критериям. По этиологии можно провести разделение на атеросклеротические, сифилитические и ревматические пороки сердца, а также пороки в исходе бактериального эндокардита.
Классификация может проводиться и по степени выраженности порока: различают пороки с высокой или умеренной степенью нарушения внутрисердечной гемодинамики или пороки без влияния на гемодинамику. По общему состоянию гемодинамики выделяют компенсированные, субкомпенсированные и декомпенсированные пороки сердца.
При классификации пороков учитывается и их локализация. К моноклапанным порокам относятся аортальный порок сердца, трикуспидальный порок, митральный порок сердца. Такие клапанные пороки сердца характеризуются поражением только одного из клапанов. Комбинированный клапанный порок сердца связан с поражением обоих клапанов.
К комбинированным порокам относятся митрально-аортальный, митрально-трикуспидальный, аортально-митрально-трикуспидальный порок и другие виды пороков. Если у больного незначительный порок сердца, признаки могут не проявляться длительное время. При гемодинамически значимых пороках появляются такие признаки порока сердца, как одышка, цианоз (посинение) кожи, отеки, учащенное сердцебиение, боли в области сердца, кашель.
Но для точной диагностики необходимо применять такие методы исследования, как ЭХО-кардиоскопия с доплерографией. Этот метода позволит выявить врожденные и приобретенные пороки сердца у детей и взрослых, оценить выраженность порока и степень его декомпенсации. Диагноз порок сердца накладывает определенный отпечаток на образ жизни человека.
При пороке сердца вредны физическое напряжение, высокие нагрузки, профессиональный спорт
Порок сердца требует вести рациональный образ жизни, уделяя внимание профилактике эндокардита, недостаточности кровообращения и нарушений ритма сердца, к которым склонны больные с пороком
Врачам известно, что порок сердца и беременность матери связаны между собой. Для предотвращения врожденных пороков необходимо тщательно наблюдать и охранять плод во время беременности, заниматься профилактикой вирусных инфекций (особенно краснухи и цитомегаловируса), получать качественное и сбалансированное питание без консервантов. А своевременное лечения очагов инфекции и предупреждение ревматизма и бактериального эндокардита поможет предотвратить приобретенный порок сердца.
Физиотерапия

В лечении врожденных пороков сердца немаловажную роль играют и физические факторы. Цели физиотерапии у детей с данным диагнозом следующие:
- уменьшение кислородного голодания (гипоксии) органов и тканей организма;
- активизация процессов торможения в головном мозге;
- стимуляция работы иммунной системы;
- повышение общего тонуса организма; при наличии очагов хронической инфекции – устранение их.
В качестве антигипоксических методов используют:
- хлоридно-натриевые ванны (улучшают функционирование симпатико-адреналовой системы, что приводит к повышению уровня в крови особых веществ – макроэргов, которые с кровотоком распространяются по всему организму и насыщают ткани; концентрация действующего вещества в ванне составляет до 10 г/л, температура воды – 36 °С; процедуры показано проводить ежедневно по 12-15 минут каждую, лечебный курс состоит из 10 воздействий);
- кислородные ванны (кислород через дыхательные пути и кожу попадает в организм больного, проникает в кровь, в результате этого улучшается снабжение им страдающих от гипоксии органов и тканей, в частности, головного мозга и сердечной мышцы; вода в ванне должна иметь температуру 36 °С, принимают ванны продолжительностью до 12 минут каждый день, курсом в 7-10 воздействий);
- углекислые ванны (углекислый газ, попадая в кровоток, воздействует непосредственно на дыхательный центр, расположенный в головном мозге;
Это приводит к урежению и углублению дыхания, что влечет за собой компенсаторное усиление диффузии кислорода в легких и повышение уровня его в крови; кроме того, данный вид физиолечения улучшает работу сердца за счет снижения потребления кислорода миокардом и активизации тока крови в венечных сосудах;
В дополнение к вышеуказанным эффектам углекислые ванны повышают устойчивость больного к физическим нагрузкам; начинают курс лечения с концентрации газа 0.7 г/л, постепенно увеличивают ее до максимума – 1.4 г/л; вода должна быть теплой (температура – 36 °С); проводят процедуры 1 раз в день по 6-10 минут курсом в 7 воздействий).
С успокаивающей целью больному назначают:
- йодобромные ванны (ионы брома попадают с током крови в головной мозг; это способствует нормализации баланса процессов возбуждения и торможения в нем;
- азотные ванны (пузырьки азота осаждаются на коже, что приводит к чуть заметному ее механическому раздражению; последнее и влечет за собой активизацию процессов торможения в коре головного мозга;
Температура воды стандартная – 36 °С, сеансы проводят каждый день по 8-10 минут; лечебный курс состоит из 10 воздействий).
Для стимуляции функций системы иммунитета применяют:
- воздушные ванны (ткани насыщаются кислородом, что способствует активизации клеточного дыхания и процессов обмена веществ, а результатом этого становится нормализация функций иммунной системы; кроме того, данный вид физиолечения повышает устойчивость организма ребенка к стрессам и всевозможным внешним повреждающим факторам);
- гелиотерапию или солнечные ванны (под воздействием ультрафиолетовых лучей в коже активизируется ряд физиологических процессов, в конечном итоге приводящих к повышению всех видов иммунитета);
- ингаляции препаратов-иммуномодуляторов (применяют растворы левамизола, лизоцима, женьшеня, экстракта алоэ; продолжительность 1 ингаляции – до 10 минут каждый день; лечебный курс состоит из 7-10 ингаляций).
Чтобы справиться с инфекцией при наличии хронических очагов ее в организме, используют:
- местное ультрафиолетовое облучение короткой длины волны (на область миндалин и глотки);
- общее ультрафиолетовое облучение средней длины волны в субэритемных дозах.
Какие причины способствуют развитию порока сердца
Развитие приобретенного порока сердца происходит следующим образом. Первопричинное заболевание провоцирует нарушение физиологической структуры клапанов. Такие нарушение бывают следующего характера:
- Сращение створок или их ригидность приводит к уменьшению просвета и называется стенозом. При таком течении приобретенного порока возрастает механическое препятствие и увеличивается сопротивляемость току крови. Часть крови после выброса возвращается назад, увеличивая нагрузку на сердечные камеры, заставляя их работать с дополнительной силой. Это провоцирует увеличение мышечной ткани камер, увеличивая их объем.
- Деформация, укорочение рубцового характера (сморщенные, разрушенные створки), которое вызывает неполное их смыкание, называется недостаточностью. В створках идет воспалительный процесс, повреждая их. Так, появляются рубцы. Гипертрофированные участки, в которых происходят дистрофические процессы, уменьшают работоспособность.
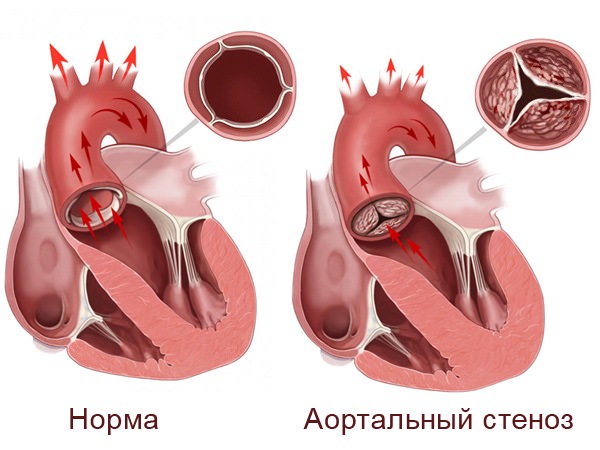
Что такое порок сердца
Каждый орган нашего тела создан, чтобы рационально действовать в системе, для которой он предназначен. Сердце относится к системе кровообращения, помогает движению крови и насыщаемостью её кислородом (О2) и углекислым газом (СО2). Наполняясь и сокращаясь, оно «проталкивает» кровь дальше, в крупные, а затем и мелкие сосуды. Если обычное (нормальное) строение сердца и его крупных сосудов нарушено – либо ещё до появления на свет, либо после рождения как осложнение болезни, то можно говорить о пороке. То есть порок сердца – это отклонение от нормы, мешающее продвижению крови, либо изменяющее её наполнение кислородом и углекислым газом. Конечно, в результате возникают проблемы для всего организма, более или менее выраженные и разной степени опасности.
Немного о физиологии кровообращения
Сердце человека, как и всех млекопитающих, разделено плотной перегородкой на две части. Левая перекачивает артериальную кровь, она ярко-красного цвета и богата кислородом. Правая – венозную кровь, она более тёмная и насыщена углекислым газом. В норме перегородка (её называют межжелудочковой) не имеет отверстий, а кровь в полостях сердца (предсердия и желудочки) не смешивается.
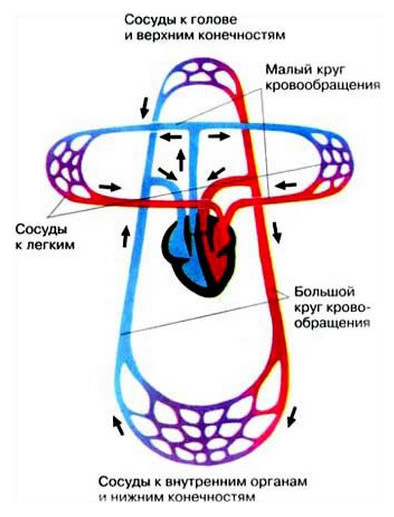 Венозная кровь от всего тела поступает в правое предсердие и желудочек, затем – в лёгкие, где отдаёт СО2 и получает О2. Там она превращается в артериальную, проходит левое предсердие и желудочек, по системе сосудов достигает органов, отдаёт им кислород и забирает углекислый газ, превращаясь в венозную. Дальше – снова в правую часть сердца и так далее.
Венозная кровь от всего тела поступает в правое предсердие и желудочек, затем – в лёгкие, где отдаёт СО2 и получает О2. Там она превращается в артериальную, проходит левое предсердие и желудочек, по системе сосудов достигает органов, отдаёт им кислород и забирает углекислый газ, превращаясь в венозную. Дальше – снова в правую часть сердца и так далее.
Система кровообращения замкнута, поэтому её называют «круг кровообращения». Таких кругов два, в обоих задействовано сердце. Круг «правый желудочек – лёгкие – левое предсердие» называется малым, или лёгочным: в лёгких венозная кровь становится артериальной и передаётся дальше. Круг «левый желудочек – органы – правое предсердие» называется большим, проходя по его маршруту, кровь из артериальной снова превращается в венозную.
Функционально левое предсердие и желудочек испытывают высокую нагрузку, ведь большой круг «длиннее», чем малый. Поэтому слева нормальная мышечная стенка сердца всегда несколько толще, чем справа. Крупные сосуды, входящие в сердце, называются венами. Выходящие – артериями. В норме они совершенно не сообщаются между собой, изолируя потоки венозной и артериальной крови.
Клапаны сердца расположены как между предсердиями и желудочками, так и на границе входа и выхода крупных сосудов. Чаще всего встречаются проблемы с митральным клапаном (двустворчатый, между левым предсердием и желудочком), на втором месте – аортальный (в месте выхода аорты из левого желудочка), затем трикуспидальный (трёхстворчатый, между правым предсердием и желудочком), и в «аутсайдерах» – клапан лёгочной артерии, на выходе её из правого желудочка. Клапаны в основном и задействованы в проявлениях приобретённых пороков сердца.
Какие бывают пороки сердца?
Рассмотрим классификацию, по изложению адаптированную для пациентов.
- Врождённые и приобретённые – изменения в нормальном строении и положении сердца и его крупных сосудов появились либо до, либо уже после рождения.
- Изолированные и сочетанные – изменения либо одиночны, либо множественные.
- С цианозом (т.н.з “синий”) – кожа меняет свой нормальный цвет на синюшный оттенок, или без цианоза. Различают цианоз генерализованный (общий) и акроцианоз (пальцы рук и ног, губы и кончик носа, уши).
Диагностика
Диагностика заболевания включает в себя следующие виды медицинских мероприятий:
- Эхокардиография, которая выполняется фетально. С её помощью осуществляется диагностирование признаков врождённого порока сердца ещё в период беременности.
- Фонокардиография. Фиксирование шумов для последующей их оценки.
- Проведение УЗИ сердца после рождения ребёнка.
- Электрокардиография.
- Рентген грудной клетки. Посредством рентгена представляется возможность оценивания размеров, контуров и месторасположения сердца.
- Пульсоксиметрия. Обследование, посредством которого предоставляется возможность к получению информации о содержании кислорода и его недостатка в периферийных тканях.
- Томография. Используется в случае редкого вида врождённого порока.
- Анализ крови: общий и биохимический. Благодаря анализу предоставляется возможность оценивания степени насыщения крови.
Стоит заметить, что не все вышеуказанные диагностические мероприятия проводятся для одного случая заболевания. Врач сам решает, какие анализы ему необходимы для постановки точного диагноза.
Некоторые пато- и морфогенетические механизмы ВПС у взрослых.
У многих взрослых больных с ВПС жалобы появляются относительно поздно — в юношеском и даже зрелом возрасте. Это обусловлено тем, что морфологические и функциональные изменения сердца и сосудов при ВПС не являются статичными, а постепенно прогрессируют.
Эволюция ВПС в постнатальный период обусловлена следующими основными общими механизмами:
- усугублением повышения ЛСС вследствие разрастания в легочных артериолах соединительной ткани с облитерацией их просвета;
- превращением гипертрофии миокарда из компенсаторной в патологическую;
- развитием кальциноза в измененных клапанах и миокарде патологически измененного выносящего тракта желудочка;
- разрывом хорд патологически измененных клапанов, что усугубляет их дисфункцию.
Кроме того, такие больные подвержены тромбозам как осложнению полицитемии и инфекционному эндокардиту. Легочная гипертензия характерна для многих ВПС. Ее наличие и выраженность часто определяют клинические проявления заболевания, его течение и возможность хирургической коррекции.
Повышение давления в легочной артерии обусловлено увеличением легочного кровотока и сопротивления легочных артериол вследствие повышения их тонуса (спазма) либо, что имеет место в большинстве случаев, в результате прогрессирующего склероза с облитерацией просвета.
Этиология
Аномалии анатомического развития сердца и крупных сосудов обычно формируются на 2-8-й неделе внутриутробного развития в результате нарушения эмбрионального морфогенеза и могут быть обусловлены как наследственными (генные, хромосомные, геномные, зиготические мутации), так и средовыми факторами, влияющими на развивающийся зародыш. Конкретные причины возникновения ВПС не известны.
Нередко они связаны с хромосомными аномалиями, выявляемыми при кариотипировании более чем у 1/3 больных с ВПС. Чаще всего это трисомия по хромосомам 21, 18 и 13. Помимо болезни Дауна, существует около 20 наследственных синдромов, в большинстве случаев, сопровождающихся ВПС. В общей сложности синдромальная патология обнаруживается у 6-36% больных.
Моногенная природа ВПС доказана в 8% наблюдений; около 90% наследуются многофакторно, т.е. являются результатом сочетания генетической предрасположенности и воздействия средовых факторов. Последние выступают в качестве провоцирующих, выявляющих наследственную предрасположенность при превышении «порога» их совместного действия.
Дефекты генетического кода и нарушения эмбриогенеза могут быть и приобретенными – воздействие на плод и организм матери некоторых неблагоприятных факторов (радиация, алкоголизм, наркомания), эндокринные заболевания (сахарный диабет, тиреотоксикоз), вирусные и другие инфекции, перенесенные в I триместре беременности (краснуха, грипп, гепатит В), прием лекарственных средств (препараты лития, варфарин, талидамид, антиметаболиты, антиконвульсанты).
Большое значение в возникновении патологии сердца и сосудов имеют смешанные вирусно-вирусные и энтеровирусная инфекции, перенесенные плодом внутриутробно.
Помимо этиологических, выделяются факторы риска рождения ребенка с ВПС. К ним относятся;
- возраст матери;
- токсикоз и угроза прерывания I триместра беременности;
- мертворожденные в анамнезе;
- наличие детей с врожденными пороками развития у ближайших родственников.
Количественно оценить риск рождения ребенка с ВПС в семье может только генетик, но дать предварительный прогноз и направить родителей на медико-биологическую консультацию может каждый врач.
Следует отметить, что частота ВПС у ближайших родственников больных с аномалиями сердца лишь в 2-5 раз выше по сравнению с таковой в общей популяции. У большинства детей с изолированными ВПС семейный анамнез не отягощен и набор хромосом не изменен. В связи с этим лишь в редких случаях имеет смысл отговаривать родителей, ребенок которых страдает ВПС, иметь еще одного ребенка.

Comments
(0 Comments)