Украинский журнал хирургии 322 2013
Лечение метастазов печени
В данное время химиотерапия в лечении метастаз в печени практически исчерпала себя. Чтобы убедиться в этом, достаточно набрать в интернете запрос «метастазы в печени продолжительность жизни». Что мы можем увидеть?
В среднем продолжительность жизни при лечении метастазов печени составляет 2-3 года. Это вынуждает пациентов искать более новые совершенные методы лечения метастазов в печени, например, такие как:
— радиочастотная эмболизация (введение радиоактивных микросфер в область опухолей печени); — электропорация;
— химиоэмболизация (введение лекарственных препаратов непосредственно в опухоль)
Диагностическое исследование
Вторичные образования, часто находят одновременно с первичной опухолью или через некоторое время после обнаружения первичного очага.
КТ или УЗИ печени – это одни из основных и доступных методов диагностики, благодаря которым можно визуализировать места локализации новообразований размером более 0,2 — 0,5 см, кроме этого очаги опухолей хорошо визуализируются на УЗИ с допплером. Интраоперационное УЗИ помогает выявить мелкие, не обнаруженные другими методами, патологические очаги.
КТ с контрастированием дает возможность точно определить объем непораженной паренхимы печени при планировании обширного оперативного удаления части органа. Опухоли мелкого размера можно диагностировать при помощи МРТ.
Радиочастотная эмболизация
Лечение метастазов в печени методом радиочастотная эмболизация проводится тем больным, которым противопоказано оперативное вмешательство. Для радиочастотной эмболизации необходимы микросферы, несущие в себе радиоактивную нагрузку. Размеры микросфер в диаметре не более 15-30 микрон.
После введения в организм микросферы застревают в мелких кровеносных сосудах, где несут радиоционную нагрузку на опухолевые очаги. Накопление радиации в ткани опухоли превышает накопление ее в здоровых тканях более чем в 6 раз.
В отличие от других методик, которые нужно выполнять каждые 2-3 месяца, радиочастотная эмболизация применяется всего 1 раз за весь период терапии.
Для внутриартериального облучения применяют стеклянные и резонные микросферы радиоактивного иттрия 90Y, а также изотопы 32 Р-коллоида. Перед началом лечения данным методом пациенту проводят развернутое обследование.
Химиоэмболизация
Для того чтобы у пациента была возможность в будущем пройти хирургическое лечение, перед операцией ему проводят химиоэмболизацию печеночной артерии.
В артерию печени вводят химиотерапевтические препараты, в короткий срок опухолевые очаги могут значительно уменьшаться в размерах.
Иногда при помощи химиоэмболизации удается добиться полного прекращения кровоснабжения патологических образований, что вызывает их омертвение.
Электропорация
Лечение метастазов в печени методом электропорации основывается на подаче разрядов тока на метастатические очаги, что приводит к омертвению и разрушению онкологических клеток продуктами электролиза в виде щелочи, кислоты и соединений платины.
В процессе проведения процедуры повышение температуры в тканях не превышает более 4,2 градусов. Из этого можно сделать вывод, что главная роль в данной процедуре принадлежит химическому уничтожению клеток опухоли, а не температурной составляющей.
Длительность по времени (около получаса) и необходимость вводить сразу несколько электродов диаметром 0,5-2,5 мм.
Пациентам с опухолью больших размеров перед процедурой назначают лечение с использованием химиотерапии с целью уменьшения опухолевого новообразования в размерах.
Что ждет пациента без лечения
При запущенном онкологическом процессе, через некоторое время болезнь прогрессирует в виде образования метастаз в отдаленных и рядом расположенных органах. Часто опухоли уже на первой стадии своего развития образуют вторичные образования во внутренних органах.
Вторичные образования формируются из клеток опухоли, которые отделяются от основного патологического очага и с током крови распространяются по всему организму, оседая на стенках кровеносных сосудов, тканях внутренних органов.
После этого клетки начинают активно делиться и размножаться. Новообразование прорастает в желчевыводящие протоки, у пациента может развиться состояние угрожающее жизни — механическая желтуха.
Порядок проведения химиоэмболизации
Как правило, химиоэмболизация проводится врачом-радиологом, который специализируется на манипуляциях, проводимых под рентгенологическим контролем. Перед началом лечения врач изучает функциональное состояние печени, определяет наличие цирроза, блоков в воротной вене или желчных протоках, а также других факторов, способных негативно повлиять на результат терапии. Непосредственно перед самой процедурой врач дает пациенту успокоительное средство или применяет анестезию.
- Химиоэмболизация осуществляется через маленький разрез в паховой области пациента.
- Катетер — тонкая пластиковая трубка — проводится от артерии в паху в артерию печени, которая и несет кровь к опухоли.
- Рентгеновские изображения помогают врачу найти оптимальное место для расположения катетера.
- Врач проводит инфузию — препарат химиотерапии направляют через катетер с помощью так называемых микросфер напрямую в опухоль.
Благодаря блокированию кровоснабжения рост опухоли замедляется, а введение препарата через печеночную артерию сводит к минимуму воздействие на соседние здоровые ткани и органы. Применение метода химиоэмболизации также позволяет снизить частоту побочных эффектов за счет применения меньших дозировок в сравнении с традиционной химиотерапией.
При химиоэмболизации используются различные химиотерапевтические препараты и их комбинации.
Побочные эффекты химиоэмболизации
Важно отметить, что препарат при химиоэмболизации в основном остается в печени, что снижает, однако не исключает риска развития краткосрочных побочных эффектов химиотерапии
- Чаще всего у пациентов развивается тошнота и усталость.
- Потеря волос встречается относительно редко.
Иногда процедура приводит к развитию осложнений: кровотечения или травмы артерии, ухудшению функции печени, инфекции. При первых признаках побочных эффектов необходимо обратиться к врачу, который оценит риски и потенциальные выгоды продолжения лечения.
После окончания курса химиоэмболизации может возникнуть так называемый синдром пост-эмболизации (post-embolization). Он характеризуется, помимо вышеназванных побочных эффектов, болью или легкой лихорадкой, ознобом, которые могут продлиться около недели.
- Боль возникает вследствие блокировки кровоснабжения опухоли. Эту боль можно лечить обычными обезболивающими средствами, предварительно проконсультировавшись с врачом.
- После процедуры рекомендуется в течение 2–3 дней избегать напряженной деятельности и не поднимать ничего тяжелого.
- Большинство людей может вернуться к привычному образу жизни в течение одной недели.
Химиоэмболизация обычно уменьшает размеры опухоли печени, иногда сокращает объем метастазов. Цель этого лечения состоит в том, чтобы держать опухоли под контролем в течение длительного времени.
Химиоэмболизация применяется как отдельно, так и в комплексе с другими методами лечения — традиционной химиотерапией, лучевой терапией, хирургическими операциями.
Приблизительно у 2/3 пациентов с опухолями печени хирургическое лечение невозможно из-за большого размера опухоли или ее неудачного расположения в непосредственной близости к кровеносным сосудам. Поэтому химиоэмболизация на сегодняшний день является одним из наиболее эффективных методов лечения опухолей печени.
РАК ПЕЧЕНИ ЭМБОЛИЗАЦИЯ
Эмболизация — это методика введения определенных веществ в сосуды с попыткой уменьшения или полного прекращения кровоснабжения раковых клеток.
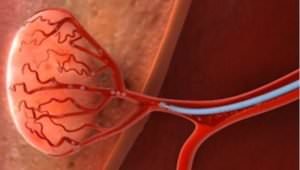
Печень — это уникальный орган, поскольку имеет два источника кровоснабжения. В норме здоровая ткань печени питается кровью от ветвей воротной вены, тогда как раковые клетки в печени обычно кровоснабжаются ветвями печеночной артерии. Данные особенности используются при лечении рака печени. Если заблокировать ветвь печеночной артерии, которая несет кровь к раковым клеткам, то это приведет к гибели опухоли. Здоровые гепатоциты затронуты не будут, поскольку получают кровоснабжение из воротной вены.
Эмболизация — это альтернативный вариант лечения пациентов, у которых опухоль не может быть удалены хирургически. Методика используется при больших размерах опухоли (обычно больше 5 см в диаметре), что исключает возможность проведения абляции. В некоторых случаях, когда размер опухоли колеблется от 3 до 5 см, эмболизация и абляция применяются совместно.
Данное лечение обычно не требует длительной госпитализации.
Артериальная эмболизация
Методика также известна под названием трансартериальная эмболизация (ТАЭ). В ходе процедуры в артерию на внутренней поверхности бедра вводится тонкая гибкая трубка (катетер), которая проводится вверх до печеночной артерии. Как правило, одновременно с этим в сосуд вводится контрастное вещество, что позволяет врачу отслеживать движение катетера с помощью ангиографии (особого вида рентгеновского исследования). Как только катетер оказывается в печеночной артерии, врач вводит в нее взвесь мелких частиц, которые закупоривают сосуд.
Процедуру эмболизации выполняют под местной или общей анестезией и под «прикрытием» антибактериальной терапии. Воротная вена должна быть проходимой. Опухоль подвергается полному или частичному некрозу.
Эмболизация уменьшает приток крови к здоровой печеночной ткани. Это может быть опасным для некоторых пациентов, которые страдают гепатитом или циррозом незатронутых раком отделов печени.
Результаты эмболизации неоднозначны. У одних больных она не даёт существенного эффекта, у других позволяет продлить жизнь. Прогноз зависит от формы опухоли, её размеров, прорастания в воротную вену, наличия асцита и желтухи . Опухоли, не имеющие капсулы, устойчивы к эмболизации . Этот метод лечения наиболее эффективен при карциноидных опухолях печени, при которых удаётся достичь значительного клинического улучшения и уменьшения их размеров.
Химиоэмболизация
Данный подход, также известный как трансартериальная химиоэмболизация, предполагает сочетание эмболизации и химиотерапии. Возможно два варианта проведения лечения.
Первая методика подразумевает использование химиопрепаратов, предварительно покрытых мелкими частицами другого вещества.
При втором подходе через катетер сперва вводится химиопрепарат, после чего просвет артерии закрывается.
Эффективность химиоэмболизации по сравнению с обычной эмболизацией изучается в клинических исследованиях.
Радиоэмболизация
Данная новая методика предполагает сочетание эмболизации и лучевой терапии.
В США она проводится путем введения в печеночную артерию мелких радиоактивных частиц под названием микросферы.
Стеклянные микросферы с иттрием-90 можно применять в качестве сильного внутреннего источника облучения опухоли, если не происходит вне-печёночного венозного шунтирования крови.
После введения данные частицы оседают в кровеносных сосудах рядом с опухолью, выделяя небольшое количество излучения в течение нескольких дней. Данное лечение доступно лишь в некоторых медицинских онкологических центрах. Долгосрочные результаты применения радиоэмболизации пока не доступны, однако известно точно, что лечение позволяет уменьшить размеры опухоли.
Другой способ доставки излучения к опухоли заключается во введении в печеночную артерию радиоактивной маслянистой субстанции под названием липиодол I-131. Данная методика радиоэмболизации сейчас проходит клинические испытания.
ГЦК нечувствительна к лучевой терапии.
ПОБОЧНЫЕ ЭФФЕКТЫ ЭМБОЛИЗАЦИИ
Возможные побочные эффекты эмболизации включают боли в животе, лихорадку, инфекционное поражение печени, воспаление желчного пузыря и образование тромбов (кровяных сгустков) в крупных сосудах печени. Серьезные осложнения возникают редко, однако возможны.
+7 495 66 44 315 — где и как вылечить рак
Химиоэмболизация фокусированная терапия против рака
В последнее время в развитых странах все шире используется метод химиоэмболизации, сочетающий в себе эмболизацию опухоли (т.е. прекращение в ней кровотока, что уже само по себе оказывает лечебное воздействие), а также доставку в её ткани химиопрепарата, который концентрируется именно в опухоли и оказывает фокусированное локальное воздействие.
Своим возникновением метод химиоэмболизации обязан ряду важных предпосылок:
1) Стремлению онкологов повысить эффективность химиотерапии, которая до сих пор остается одним из наиболее распространенных методов лечения онкологических заболеваний, особенно в тех случаях, когда речь идет о неоперабельных опухолях;
2) Осознаваемой докторами необходимости снизить концентрацию химиопрепарата в здоровых тканях организма при сохранении высокой концентрации в тканях опухоли;
3) Развитию технологии обычной эмболизации различных сосудистых бассейнов — от аневризм головного мозга и миомы матки, до варикоцеле и кровоточащих сосудов при травме;
4) Совершенствованию эндоваскулярного инструментария, который сейчас позволяет вводить катетеры и микрокатетеры (и доставлять эмболизационный препарат) в самые отдаленные сосудистые бассейны.
Еще в конце 20 века исследователи искали ответ на вопрос «Есть ли возможность доставить химиопрепарат непосредственно в опухоль без вреда для пациента? » И уже в начале 80-х годов был разработан метод масляной химиоэмболизации опухолей, при котором смесь рентгеноконтрастного масляного препарата и средства для химиотерапии вводится в артерию, питающую опухоль. К сожалению, эффективность этого метода оставалась довольно невысокой, во многом потому что концентрированное воздействие на опухоль носит кратковременный характер, а масляный препарат не прекращал кровоток в ткани самой опухоли. При этом у масляной химиоэмболизации сохраняется и главный недостаток химиотерапии — токсическое воздействие на организм.
К сожалению, из-за относительно дешевизны масляного препарата его до сих пор нередко используют в нашей стране, хотя его эффективность при лечении, например, метастазоврака кишечника в печень (а это одна из самых распространенных ситуаций, когда нужна химиоэмболизация), не подтверждается данными исследований. Таковой ситуация оставалась до начала 21 века, когда развитие технологий позволило разработать специальные микросферы — сферические частицы, способные накапливать химиопрепарат, а потом высвобождать его в течение длительного времени. При этом они также блокируют кровоток в самой ткани опухоли, действуя подобно частицам для эмболизации маточных артерий, например.
Сейчас в мировой практике активно применяются два типа таких препаратов, имеющих ряд отличий. Это препарат DC Bead (произносится «ди-си бид»), который производится компанией Biocompatibles. Его распространением на территории Европы, включая и Россию, занимается японская компания Terumo — один из лидеров в области инновационного оборудования для эндоваскулярной хирургии и онкологии. Вторым препаратом является препарат Hepaspheres, выпускаемый компанией Biosphere Medical, являющейся подразделением американской медицинской компании Merit Medical.

Comments
(0 Comments)