Вторичный гемохроматоз
Распространенность
Обычно медики используют понятие «гемохроматоз» для описания именно генетической мутации, поскольку вторичный синдром накопления железа наблюдается в разы реже, чем наследственный. Результаты статистических исследований предрасположенности людей к развитию заболевания вывели гемохроматоз из ряда редких патологий. Оказалось, что средняя частота распространения составляет 0,03–0,07% случаев на население, причем в этнических группах эта цифра больше, чем для негроидной расы.
По данным ВОЗ 10% всех людей на планете имеют предрасположенность к развитию гемохроматоза, а в России эта цифра составляет не менее 1%. Было установлено, что в США из 250 млн населения к развитию болезни склонны 1 млн, а диагностирована она у 150 тыс. человек.
Гемохроматоз причины
Как и многие заболевания, гемохроматоз можно разделить на первичный (он же наследственный или идиопатический гемохроматоз), и на вторичный (появляется как следствие заболеваний или воздействии на орган неблагоприятных факторов).
Первичный гемохроматоз (он же идиопатический гемохроматоз) является основной разновидностью этого заболевания. Причины, которые запускают его появление сугубо генетические. Возникает ошибка в определенных хромосомных локациях и организм человека начинает поглощать железо в непомерных количествах. Для сравнения нужно сказать, что в норме в организм человека с помощью клеток тонкого кишечника всасывается около 3-х грамм железа ежедневно. При гемохроматозе эта цифра увеличивается практически в двадцать раз.
Вследствие этого организму приходится куда-то утилизировать излишки железа, которое не используется им для метаболических целей. Как и в природе, организм идёт по самому простому пути: излишнее количество какого-либо вещества он просто превращает в отложения. В случае с гемохроматозом возникают отложения железа. Если точнее сказать, то железо будет всасываться клетками тонкого кишечника и постепенно трансформироваться в пигмент гемосидерин. Ненужное организму количество этого самого пигмента и будет засорять клетки органов.
Самыми частыми органами, куда организм будет прятать лишнее количество железа, станут печень, а за ней и поджелудочная железа. Кроме вышеназванных органов, также излишним железом будет постепенно заполняться сердечная мышца. Конечно же, чужеродные «залежи железа» в органах не будут позитивно влиять на работу этих органов. Хуже того, отложения излишков железа постепенно губят клетки. Позднее, на месте погибшей клетки разрастается соединительная ткань, пытаясь заместить умершую структуру.
Важно знать, что гемохроматоз является так называемым «заболеванием накопления», иными словами гемохроматоз проявится только тогда, когда в организме будет присутствовать определённое количество излишков железа или его отложения запустят изменения в органах. Поэтому одним их классических признаков гемохроматоза будет необходимость в достаточно длительном течении для полного раскрытия развернутой клинической картины (иногда процесс развития гемохроматоза может затянуться на десятилетия)
Вторичные варианты гемохроматоза обычно появляются при запущенных циррозах печени
Механизм появления этого вида гемохроматоза объясняется тем, что цирротически повреждённая печень не синтезирует важное вещество — трансферрин. Это вещество является основанным транспортом, который доставляет железо в те места, где оно нужно для синтеза различных новых структур и клеток (например, новых эритроцитов)
Так как транспортировать железо нечему, или количество вещества — транспорта является недостаточным, то постепенно количество железа увеличивается, организм попытается «спрятать» неиспользующееся железо и появляется картина уже известного нам гемохроматоза.
Также вторично обусловленный гемохроматоз может развиться из-за постоянного употребления алкоголя. Спиртное очень хорошо стимулирует захват железа в полости тонкой кишки, и может подстегнуть появление наследственного гемохроматоза. Кстати, чаще всего, когда хотят сказать о возможном наличии гемохроматоза у больного, то априори подразумевают именно наследственный гемохроматоз. Вторичные гемохроматозы появляются не так часто, если сравнивать их с наследственными видами.
Гемохроматоз лечение
Так как гемохроматоз в первую очередь является заболеванием генетического типа, то лечения направленного непосредственно на саму причину его возникновения ещё пока нет. Но разработан целый комплекс мер, направленный на уменьшение клинических проявлений, снижение риска появления осложнений и облегчения состояния больного. Этот комплекс включает в себя специальную диету, методы по экстракорпоральной фильтрации крови, медикаментозные препараты, микрохирургические манипуляции.
Диета при гемохроматозе играет важную роль в лечении больного. Полностью удаляются из рациона те продукты, которые являются донорами железа для человеческого организма. В большей мере это касается мясных продуктов. Больным с гемохроматозом строго запрещено употребление алкоголя в любых количествах (механизм воздействия алкоголя на повышение содержания железа в организме рассмотрен выше).
Одним из самых эффективных методов по купированию развития гемохроматоза является кровопускание. Благодаря ему, в организме значительно снижается уровень лишних железосодержащих веществ. У больных гемохроматозом средняя частота проведения этой процедуры будет составлять около 2-х раз в неделю. Обычно за одну процедуру выпускается средний для неё объём крови (около 450 мл).
Но чаще всего график кровопускания составляется индивидуально для каждого больного гемохроматозом. Учитываются показатели избытка железа, уровень гемоглобина на момент начала процедур. Чаще всего эти процедуры будут проводить до тех пор, пока анализы не покажут наличие у больного анемии 1-й (лёгкой) степени.
Ещё одним методом очищения организма от излишков железа является более современная процедура цитофереза. В ходе этой процедуры кровь будут пропускать по специальному замкнутому контуру с последующим её возвратом в родное кровяное русло. Но при этом часть крови будет удаляться: чаще всего забирают именно её клеточную составляющую, а плазму не трогают. В среднем проводят около 10 таких процедур одним циклом.
После вышеописанных процедур также можно применять введение медикаментозных средств, которые связывают и удаляют железо из организма. Чаще других здесь будет использоваться Десферал в виде капельниц. Десферал и его производные относят к так называемым “хелатным” препаратам. Их химическая формула подобна двум клешнями, которые захватывают и выводят токсические вещества.
Важно знать, что начало лечения гемохроматоза напрямую будет зависеть от появления его клинических проявлений: чем они будут ярче выражены, тем сильнее будет медикаментозная поддержка. Рекомендуем к прочтению: http://vlanamed.com
Рекомендуем к прочтению: http://vlanamed.com
Что такое фокальная нодулярная гиперплазия печени
Под гиперплазией подразумевается патологический рост клеток ткани того или иного органа. Соответственно, нодулярная гиперплазия печени – это патологический рост тканей печеночной паренхимы. Проще говоря, это доброкачественная опухоль печени, не имеющая капсулы.
Характеристика
Фокальная нодулярная гиперплазия печени представляет собой плотное новообразование округлой формы. Основу центральной части опухоли представляет соединительная ткань, периферическая часть представлена гепатоцеллюлярной тканью. Узел также содержит пролиферирующие желчные протоки. Границы образования четкие, легко определяющиеся при компьютерных методах диагностики.
Как правило, новообразование сохраняет доброкачественный характер, однако возможна злокачественная трансформация.
Симптомы
При данном заболевании возможно бессимптомное течение. Проявляющиеся симптомы выглядят следующим образом:
- дискомфорт в проекции печени;
- тошнота и диспепсические расстройства;
- слабость и повышенная утомляемость.
Данные проявления ничем не отличаются от большинства заболеваний печени, поэтому без специфической диагностики здесь не обойтись.
Диагностика
Гиперплазию можно определить еще на этапе осмотра у врача при пальпации – в районе правого подреберья прощупывается объемное образование. Однако многое зависит и от локализации опухоли, поэтому наиболее достоверными методами считаются:
- ультразвуковое исследование (УЗИ);
- магнитно-резонансная томография (МРТ);
- компьютерная томография (КТ);
- биопсия ткани печени;
- биохимический анализ крови.
В ходе компьютерной визуализации фокальная нодулярная гиперплазия печени определяется в виде расходящихся узелков, размеры которых в зависимости от стадии развития патологии могут варьироваться от 1 до 15 сантиметров. В отличие от обычной аденомы узлы имеют больший размер и выраженный сосудистый рисунок.
Для дифференциальной диагностики узловой гиперплазии и гепатоаденомы сканирование печени обычно сочетают с артериографией.
Возможные причины
Этиология данного заболевания до сих пор окончательно не выяснена. Наиболее вероятной причиной возникновения доброкачественного новообразования в печени считается применение гормонов. У женщин это обычно противозачаточные средства, а у мужчин – анаболические стероиды и препараты тестостерона.
Чаще всего такие андрогены как пропионат тестостерона или тестэнат используются для лечения половой слабости и сперматогенеза у мужчин. Данные препараты стимулируют выработку мужского гормона тестостерона, который не только улучшает сексуальную функцию, но и усиливает синтез белка. И в этом состоит главная загвоздка. Для спортсменов рост силы и мышечной массы (ведь именно из белка состоят наши мышцы) является неоспоримым плюсом, а вот побочное действие – рост патологических новообразований – уже является серьезным минусом. Таким образом, гормональные сдвиги способны спровоцировать фокальную нодулярную гиперплазию печени.
Лечение
Если гиперплазия носит доброкачественный характер (как и бывает в большинстве случаев), специфического лечения не требуется, однако при приеме гормональных препаратов велика вероятность того, что придется их отменить – это помогает не только избежать дальнейшего роста новообразования, но даже помогает достичь ремиссии.
В любом случае необходим регулярный контроль состояния узлов при помощи УЗИ или МРТ.
Оснований для паники в данном случае нет, поскольку печень обладает хорошими регенеративными способностями. Медицине известны случаи полного восстановления ткани даже при удалении 70% печени.
Пациенту также необходимо сократить количество белка в рационе, алкоголь при этом допускается лишь в незначительных дозах (примерно один бокал сухого вина в неделю). Также необходимо ограничение сладких, острых и копченых продуктов.
Что это такое
Гемохроматоз печени представляет собой наследственную болезнь, обусловленную некоторыми генетическими мутациями, вследствие которых нарушается обмен железа в организме человека с последующим его накоплениям в тканях. В тело железо попадает из пищи, которую человек употребляют. Органами, которые больше всего страдают из-за его переизбытка, является печень, поджелудочная железа, миокард, селезенка, кожа и эндокринные железы. Из-за этого во всех них со временем начинают развиваться другие болезни вторичного характера.
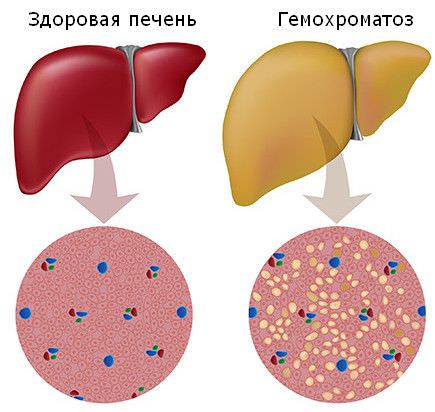
Гемохроматоз печени имеет несколько названий, которые являются идентичными друг другу. Данное заболевание часто называют пигментным циррозом или бронзовым диабетом, сидерофилией или синдромом Труазье-Ано-Шоффара.
Последние данные по статистике говорят, что в Соединенных Штатах примерно 1 миллион человек предрасположены к гемохроматозу. Всего лишь 150 тысяч из этих 1 миллиона имеют соответствующий диагноз. Можно предположить, что вероятность развития заболевания у человека составляется всего 0,33%.
На данный момент примерно 10% населения Земли имеют в своей ДНК рецессивные гены гемохроматоза печени. Больше всего от этого заболевания страдают жители Ирландии, из-за чего иногда его называют «кельтской болезнью».
Вопросы к специалистам
Заболевание – достаточно редкое, потому информации о его правильной терапии даже на современном этапе развития медицины не всегда достаточно. У пациентов и их родственников возникает немало вопросов по поводу правильного образа жизни пациента с гемохроматозом, эффективных методиках лечения. Мы постарались собрать самые распространенные из них.
Стоит ли применять Урсосан в лечении?
Профилактика заболеваний печени имеет первоочередное значение при постоянной терапии гемохроматоза. Препарат Урсосан прекрасно помогает печени восстанавливаться при различного рода повреждениях. Он защищает клетки печени, препятствует их разрушению по каким-либо причинам и не дает погибнуть. Урсосан эффективен в лечении цирроза, что подтверждается многочисленными исследованиями. Также он необходим в случаях, где требуется восстановить функциональный потенциал печени, уменьшить фиброобразование.
Как еще можно снизить уровень железа?
Пациентам с гемохроматозом нужна диета, в которой будет минимальное количество железосодержащих компонентов. Также не стоит потреблять витамин С, так как он способствует повышению уровня железа. Примечательно, что этого витамина много в таблетках и микстурах, капсулах и растворах, поэтому прием любого лекарства нужно обсуждать с врачом. Не стоит употреблять красное мясо, ливер и потроха, гранат, листья шпината, лимоны, киви, морепродукты.
Внимание: если у Вас есть другие вопросы, задайте их нашему специалисту прямо сейчас!
Можно ли больному употреблять алкоголь?
Этот вопрос решается индивидуально с лечащим врачом. Конечно, пациенты, у которых из-за гемахроматоза развились сопутствующие заболевания печени, не могут употреблять алкоголь.
А если беременность?
Пациентками женского пола с гемохроматозом в случае положительного теста на беременность нужно обратиться к врачу. Если отца будущего ребенка есть нарушения на генетическом уровне, то будущую маму нужно будет дополнительно обследовать. Тем не менее, заболевание не является опасным для вынашивания плода или дальнейших родов.
Можно ли быть донором?
При гемахроматозе кровь не может быть источником данного заболевания. Ни один из компонентов крови не поврежден. Наследственные заболевания при переливании крови не передаются. Донора нужно обследовать на наличие других болезней.
Что делать, если в семье есть случай гемохроматоза?
Вероятность наличия недуга у родственников, относящихся к первому колену, составляет порядка 25%. Нужно для собственной безопасности проводить регулярные обследования в возрасте 18-30 лет. Это позволит в случае развития гемохроматоза выявить его на ранней стадии.
Метаболизм железа
Общее содержание железа в организме составляет примерно 4—5 г. Из этого количества 60% приходится на гемоглобин, 10% — на миоглобин, цитохромы, каталазу и пероксидазу; менее 1% приходится на железо, связанное с трансферрином, миоцитах и клетках других органов. Примерно треть этих запасов приходится на печень, главным образом на ферритин, и является внутренним резервом железа, расходуемым при необходимости.
Всасывание железа. Здоровый взрослый в среднем потребляет 10—15 мг железа в сутки. Лишь 10% этого количества всасывается в двенадцатиперстной и проксимальной части тощей кишки. Железо гема, содержащееся в мясе, всасывается в 4 раза лучше, чем неорганическое, входящее в состав овощей и круп. Не существует какого-либо физиологического механизма удаления железа из организма в значимом количестве. Поэтому в норме всасывание железа в кишечнике строго регулируется, чтобы обеспечивать лишь количество, необходимое для покрытия его потерь со слушивающимися клетками эпителия ЖКТ и кожи, а у женщин также с менструальной кровью. В сутки мужчина теряет I мг железа, а женщина 1,5 мг.
Гемохромaтоз печени
Гемохроматоз печени – генетическое аутосомно-рецессивное заболевание, характеризующееся повышенным всасыванием и отложением железа в печени и других паренхиматозных органах. В клинике гемохроматоза печени превалирует триада признаков: цирроз, гиперпигментация кожных покровов, эндокринные нарушения.
Диагностика основана на изучении семейного анамнеза, выявлении нарушений обмена железа, МРТ печени с последующей биопсией, выявлении гомозиготного носительства гена гемохроматоза. Специфическое лечение гемохроматоза печени включает назначение препаратов, выводящих излишки железа из организма, эфферентные методики – кровопускание, цитаферез.
Заболевание неизлечимо.
Гемохроматоз печени – наследственное заболевание, при котором происходит нарушение метаболизма железа в организме, его избыточное отложение в органах и тканях. Несмотря на системный характер нарушений, наиболее тяжело при гемохроматозе поражается печень – в ней развиваются цирротические изменения.
Отложение железа в коже проявляется гиперпигментацией, в железах внутренней секреции – эндокринными нарушениями, сахарным диабетом. Впервые гемохроматоз печени был описан в 1871г., с тех пор исследования в этой области не прекращаются.
На сегодняшний день выявлен ген, отвечающий за развитие гемохроматоза, связанный с HLA-комплексом гистосовместимости. Ген этот рецессивный, поэтому для появления клиники гемохроматоза необходимо наличие данной мутации у обоих родителей пациента.
Гемохроматоз печени – заболевание редкое, гетерозиготное носительство встречается у 10% населения, а гомозиготность – лишь в 0,3%. Мужчины страдают гемохроматозом печени в десять раз чаще женщин.
Лечение и прогноз гемохроматоза печени
Методов полного излечения гемохроматоза печени в гастроэнтерологии не существует, поэтому терапия направлена на купирование симптомов заболевания. Для начала назначается диета с пониженным содержанием железа и повышенным уровнем белка. В последующем используются методики, позволяющие усилить выведение железа из организма.
Наиболее доступный способ уменьшить пул железа – кровопускание. Для правильного расчета объема кровопускания учитываются уровни гемоглобина, гематокрита, трансферрина. При заборе 500 мл крови теряется 200-250 мг железа. В среднем производится эксфузия 300 мл крови дважды в неделю.
Более сложным методом, требующим специального оборудования, является цитаферез – при этом осуществляется удаление клеточных элементов, а плазма возвращается в кровяное русло. Сеансы кровопусканий или цитафереза проводятся до развития у больного гемохроматозом печени умеренной анемии.
Так как на фоне исходной анемии использование эфферентных методик ограничено, то в качестве подготовки и сопровождения цитафереза назначается рекомбинантный эритропоэтин. Данный препарат усиливает утилизацию железа, благодаря чему снижается его концентрация в тканях, повышается гемоглобин.
Курс введения эритропоэтина – 10-15 недель.
Течение заболевания длительное, а прогноз благоприятный лишь при своевременном начале лечения.
Если патогенетическая терапия была инициирована до значительной перегрузки организма железом, развития цирроза, диабета и полиорганной недостаточности – выживаемость увеличивается на несколько десятилетий.
В случае развития цирроза риск гепатоцеллюлярной карциномы возрастает в 200 раз. Смерть обычно наступает от печеночной недостаточности и ее осложнений. Профилактики гемохроматоза печени не существует.
Диагностика Гемохроматоза
Особенности диагностики:
Диагностика основывается на множественных органных поражениях, случаях заболевания у нескольких членов одной семьи, повышенном содержании железа, экскреции железа с мочой, высокой концентрации трансферрина, ферритина в сыворотке крови. Диагноз вероятен при сочетании с сахарным диабетом, кардиомиопатией, гипогонадизмом и типичной кожной пигментацией. Лабораторными критериями служат гиперферремия, повышение индекса насыщения трансферрина (более 45 %). Резко увеличиваются уровень ферритина в сыворотке крови, экскреция железа с мочой (десфераловая проба). После внутримышечного введения 0,5 г десферала выделение железа возрастает до 10 мг/сут (при норме 1,5 мг/сут), коэффициент НТЖ (железо/ОЖСС) повышается. С внедрением в практику генетического тестирования увеличилось количество лиц с наличием гемохроматоза без клинических признаков перегрузки железом. Проводят исследование на наличие мутаций C282Y/H63D в группе риска по развитию перегрузки железом. Если пациент является гомозиготным носителем C282Y/H63D, диагноз наследственного гемохроматоза может считаться установленным.
Среди неинвазивных методов исследования депонирование микроэлемента в печени может быть определено с помощью МРТ. В основе метода лежит снижение интенсивности сигнала печени, перегруженной железом. При этом степень снижения интенсивности сигнала пропорциональна запасам железа. Метод позволяет определить избыточное отложение железа в поджелудочной железе, сердце и других органах.
При биопсии печени наблюдается обильное отложение железа, дающего положительную реакцию Перлса. При спектрофотометрическом исследовании содержание железа составляет свыше 1,5 % от сухой массы печени
Важное значение придается количественному измерению уровня железа в биоптатах печени методом атомно-абсорбционной спектрометрии с последующим исчислением печеночного индекса железа. Индекс представляет соотношение концентрации железа в печени (в мкмоль/г сухого веса) возрасту больного (в годах)
При ПГХ уже на ранних стадиях этот показатель равен или превышает 1,9-2,0 и не достигает указанной величины при других состояниях, характеризующихся гемосидерозом печени.
В латентной стадии заболевания функциональные пробы печени практически не изменяются, а по данным гистологического исследования, наблюдаются гемосидероз 4-й степени, фиброз портальных трактов без выраженных признаков воспалительной инфильтрации.
На стадии развернутых клинических проявлений гистологические изменения печени обычно соответствуют пигментному септальному или мелкоузловому циррозу с массивными депозитами гемосидерина в гепатоцитах и менее значительными в макрофагах, эпителии желчных протоков.
При гистологическом исследовании в терминальной стадии заболевания выявляется картина генерализованного гемосидероза с поражением печени (по типу моно- и мультилобулярного цирроза), сердца, поджелудочной, щитовидной, слюнных и потовых желез, надпочечников, гипофиза и других органов.
Перегрузка железом наблюдается при ряде врожденных или приобретенных состояний с которыми необходимо дифференцировать ПГХ.
Классификация и причины развития состояния перегрузки железом:
- Семейные или врожденные формы гемохроматоза:
- Врожденный HFE-ассоциированный гемохроматоз:
- гомозиготность по C282Y;
- смешанная гетерозиготность по C282Y/H63D.
- врожденный HFE-неассоциированный гемохроматоз.
- Ювенильный гемохроматоз.
- Перегрузка железом у новорожденных.
- Аутосомно-доминантный гемохроматоз.
- Врожденный HFE-ассоциированный гемохроматоз:
- Приобретенная перегрузка железом:
- Гематологические заболевания:
- анемии на фоне перегрузки железом;
- большая талассемия;
- сидеробластная анемия;
- хронические гемолитические анемии.
- Гематологические заболевания:
- Пищевая нагрузка железом.
- Хронические заболевания печени:
- алкогольная болезнь печени;
- неалкогольный стеатогепатит.
Заболевание необходимо также дифференцировать с патологией крови (талассемия, сидеробластная анемия, наследственная атрансферри-немия, микроцитарная анемия, поздняя кожная порфирия), заболеваниями печени (алкогольное поражение печени, хронический вирусный гепатит, неалкогольный стеатогепатит).
Патофизиология наследственного гемохроматоза, вызванного мутациями гена HFE
Открытие связи между геном HFE и гемохро-матозом послужило стимулом для изучения его роли в нарушении обмена железа. Помимо того что при гемохроматозе, вызванном мутациями гена HFE, снижена экспрессия гепсидина, белок HFE обнаруживается в энтероцитах крипт двенадцатиперстной кишки, где он связан с β2-микроглобулином и рецепторами трансферрина. Есть предположения, что белок HFE облегчает опосредованный рецепторами трансферрина захват железа клетками крипт, а продукт мутантного гена HFE этой способностью не обладает, что приводит к относительному дефициту железа в клетках крипт. В свою очередь, это может увеличивать экспрессию белка DMT1 — переносчика двухвалентных катионов, который отвечает за всасывание железа в двенадцатиперстной кишке.
Диагностика гемохроматоза
Подозрение на гемохроматоз возникает в том случае, если анализы показывают очень высокий уровень железа в крови. Для подтверждения диагноза определяют содержание железа в ткани печени, для чего делается биопсия печени. Необходимо также обследование и близких родственников больного — отца, матери, братьев и сестер.
Исход болезни зависит от своевременной диагностики и проведения соответствующего лечения. Если человек унаследовал ген, который вызывает гемохроматоз, лечение нужно начать как можно раньше, пока печень еще не повреждена. В случаях, когда диагноз был поставлен до развития цирроза, при соблюдении всех врачебных рекомендаций возможен благоприятный прогноз заболевания.
Диагноз основывается на учете меланодермии (серовато-коричневого цвета), гепатомегалии, гиперферремии (более 40 мкм/л), гиперферритинемии (более 300 мкг/л), поражении миокарда, артропатии. Уточняется гистологическим исследованием биоптатов печени с окраской на железо (отложение железа в гепатоцитах и купферовских клетках).
Гемохроматоз симптомы
У гемохроматоза симптомы напрямую связаны с органами, которые повреждают накопившиеся там «железные» отложения. Кстати, еще интересный факт: чаще всего гемохроматоз начинает клинически разгораться где- то приблизительно в сорокалетнем возрасте (о причинах такого течения уже было написано выше: все дело во времени накопления ненужного железа). Здесь также важную роль играет пол: мужчины составляют основной контингент больных гемохроматозом. Женщин спасают их функциональные особенности: каждый месяц, с менструацией может выходить определённое количество лишнего железа.
При «захламлении» печени гемосидериновыми отложениями может появиться ярчайшая клиника цирроза. Это и понятно: при гемохроматозе печень является ёмкостью для постоянного сбрасывания организмом ненужного железа, которое пагубно влияет на её составляющие. Развивается гемохроматоз печени.
Постепенно исчезают поврежденные клетки печени. Их пытается заместить соединительная ткань. Из-за этих процессов печень теряет и свою форму, постепенно уменьшаясь в размерах, и достаточный уровень своих функций. Появляются все «прелести» цирроза: появление асцита, расцвет портальной гипертензии и зависшая угроза смерти от кровотечения из варикозно расширенных вен пищевода.
Когда таким же повреждениям подвергается поджелудочная железа, то результат не менее плачевный. Из-за постоянных отложений железа умирают одни из самых важных для организма и жизни человека клеток — клетки поджелудочной железы. Постепенно исчезают В-клетки, которые занимаются постоянным синтезированием инсулина. В результате, гемохроматоз может запустить появление вторичного сахарного диабета и всех его последствий. Кстати, одно из названий гемохроматоза, а именно «бронзовый» сахарный диабет, появилось именно из этого клинического проявления.
Этот характерный бронзоватый оттенок у больных гемохроматозом появляется благодаря тому, что в верхнем слое кожи накапливается все тот же печально известный гемосидерин. И получается вся палитра бронзовых оттенков на коже у больных: от дымчатой до насыщенно — бронзовой окраски.
Лучше всего эти цветовые явления проявляются на открытых участках тела: лице и руках. При более детальном осмотре такую окраску можно найти в области подмышечных впадин и наружных половых органах.
Когда при гемохроматозе повреждаются клетки сердечного мышечного слоя, то появится гемохроматозная кардиомиопатия. Она будет проявляться тем, что камеры сердца будут растягиваться, сердце увеличится в своих размерах. Эти изменения запустят постоянные нарушения ритма и станут причиной всем известной сердечной недостаточности. Это одно из самых грозных проявлений гемохроматоза. Если его не корректировать медикаментозными средствами, то именно сердечная недостаточность станет причиной летальности у больных гемохроматозом (где- то около 37% больных).
Как уже описывалось выше, гемохроматоз является заболеванием с большой длительностью протекания. В среднем период протекания болезни составляет около 15-20 лет
Важно знать, что продолжительность жизни больных будет напрямую зависеть от начала проявлений цирроза печени. После того как появились его признаки, в среднем больной гемохроматозом сможет прожить ещё где-то около 10-ти лет
Диагностика
Обследование на наличие гемохроматоза лучше провести до первых его симптомов. Выявление недуга на ранней стадии позволит избежать тяжелых, часто необратимых, осложнений. Для этого нужно проанализировать кровь по таким показателям:
- Уровень железа при гемохроматозе повышен у большинства больных;
- Насыщение трансферрина – специфического белка, переносящего железо в крови(обычно показатель повышен более, чем на 45%);
- Уровень ферритина – белка, накапливающего в организме человека железо. Ее количество сильно возрастает, иногда более чем до 300 нг/мл.
 Диагностика требует еще и дифференциации заболевания от ряда других заболеваний (это может быть алкогольная болезнь печени). В зависимости от стадии и степени тяжести гемохроматоза могут понадобиться дополнительные методы диагностики. Проводят генетическое исследование, позволяющее выявить мутации в генах.
Диагностика требует еще и дифференциации заболевания от ряда других заболеваний (это может быть алкогольная болезнь печени). В зависимости от стадии и степени тяжести гемохроматоза могут понадобиться дополнительные методы диагностики. Проводят генетическое исследование, позволяющее выявить мутации в генах.
Одним из самых полезных методов можно считать биопсию. В некоторых случаях ее назначают, чтобы окончательно подтвердить диагноз. Также применяют МРТ (компьютерную томографию), чтобы выяснить степень накопления железа в печени и сердце. Дополнительно проводят количественную флеботомию. Один-два раза в неделю под контролем анализов у пациента производят забор части крови. В таком состоянии у людей без гемохроматоза начинает стремительно развиваться анемия, а если человек все-таки болен, то изменения начинаются другие.
Симптомы гемохроматоза печени
Для появления первых симптомов гемохроматоза печени обычно требуется не менее 20 лет, пока общее содержание железа в организме не превысит 20-40 г. На начальном этапе заболевания, даже при наличии генетической предрасположенности, перегрузки организма железом не наблюдается. Следующим этапом заболевания является перегрузка тканей ионами железа без клинических проявлений. И только на поздней стадии гемохроматоза печени появляются типичные клинические признаки.
Первыми проявлениями гемохроматоза печени на протяжении долгих лет могут служить лишь слабость, повышенная утомляемость, снижение половой функции у мужчин (снижение либидо и т. п.) и аменорея у женщин. Нарушение обмена железа приводит к кальцинозу суставов, трофическим изменениям в коже и хрящах, половых органах. На более поздних стадиях заболевания клиническая картина становится развернутой: отложение гемосидерина в коже сопровождается гиперпигментацией открытых мест, подмышечных впадин и промежности.
Из внутренних органов первой поражается печень: происходит некроз гепатоцитов, избыточное образование коллагена, что в будущем приводит к циррозу. Изначально печень увеличивается в размерах, становится плотной, болезненной при пальпации. В будущем, на фоне формирования цирроза, печень уменьшается, развивается симптоматика печеночно-клеточной недостаточности и портальной гипертензии.
Более чем у 80% пациентов с гемохроматозом печени отмечаются эндокринопатии: поражаются гипофиз и эпифиз, щитовидная, поджелудочная и половые железы. Практически у всех пациентов с эндокринопатиями развивается сахарный диабет, зачастую инсулинозависимый. Очень часто поражаются суставы, центральная нервная система.
Отложение гемосидерина в сердце отмечается у 90-100% больных, но клиническая симптоматика возникает не более чем у трети пациентов. Гемохроматоз сердца проявляется кардиомиопатией, гипертрофией миокарда, тяжелой сердечной недостаточностью.

Comments
(0 Comments)